Caso Clínico
Isquemia Renal en el seguimiento tras tratamiento endovascular de disección de Aorta
Renal Ischemia in the follow-up after endovascular treatment of Aortic Dissection
Actual. Med. 2018; 103: (805). Supl. 16-44
RESUMEN
La disección de aorta se trata del evento catastrófico más frecuente que afecta a la aorta, con una mortalidad de hasta el 68% en la primera semana. Su tratamiento varía en función del tipo de disección y de la presentación clínica y otras características radiológicas de la disección. Describimos el caso de una disección tipo B en un varón de mediana edad que fue tratado de manera exitosa mediante la técnica Petticoat aunque se trombosó la arteria renal derecha que surgía de falsa luz. En el seguimiento se detectó una estenosis crítica de la arteria renal izquierda acompañado de empeoramiento de la función renal. Se le colocó un stent balón-expandible en dicha arteria a través de la malla del stent e-XL. El paciente fue dado de alta sin complicaciones. Es importante un seguimiento de esta patología para detectar precozmente las complicaciones y así minimizar la morbimortalidad derivada de las mismas.
Palabras clave: disección; seguimiento; malperfusión.
ABSTRACT
Aortic dissection is the most frequent catastrophic event that affects the aorta, with a mortality of 68% in the first week. Its treatment varies according to the type of dissection, the clinical presentation and another radiological characteristics of the dissection. We describe the case of a type B dissection in a middle-aged male who was successfully treated through the Petticoat technique, although the right renal artery that arose from false lumen was thrombosed. At follow-up, a critical stenosis of the left renal artery was detected accompanied by decreasing of renal function. A balloon-expandable stent was placed in the artery through the e-XL stent. The patient was discharged without complications. It is important to monitor this pathology to detect early complications and minimize the morbidity and mortality derived from them.
Keywords: dissection; surveillance; malperfusion.
Leer Artículo Completo
INTRODUCCIÓN
La Disección Aórtica se produce con el desgarro o rotura de la íntima y de las capas internas de la media de la Aorta que permite el paso de sangre creando una luz falsa (LF) en la capa media que progresa longitudinalmente en sentido distal (más frecuentemente) y/o proximal (retrógrada).
Se trata de una urgencia médico-quirúrgica de elevada mortalidad que presenta una mortalidad del 68% en la primera semana1. La incidencia de esta patología varía entre 2,9-3,5 casos/100.000 personas/año2. Los factores que predisponen al desarrollo de una disección de aorta incluyen la edad, la hipertensión arterial y las anormalidades estructurales de la pared aórtica1.
Puede clasificarse de acuerdo a la localización anatómica del desgarro aórtico principal en: Tipo A de Stanford, donde la disección se origina en la Aorta Ascendente, y tipo B, donde la disección empieza distal al origen de la arteria subclavia izquierda3.
También puede establecerse una clasificación en función del tiempo transcurrido desde el inicio de la sintomatología. De manera que una disección se considera aguda dentro de las 2 primeras semanas del inicio de los síntomas y crónica después de 90 días. El período entre 2 semanas y 90 días se considera la fase subaguda y durante este tiempo disminuye el riesgo de muerte pero el flap intimal aún permanece flexible por lo que éste se considera el mejor momento para la cobertura endovascular del desgarro aórtico proximal causante de la disección4.
La forma de presentación más habitual es el dolor torácico (lacerante y retroesternal irradiado a espalda) e hipertensión arterial. Según su evolución, puede presentar otra sintomatología muy variada derivada del compromiso de ramas aórticas (isquemia intestinal, renal, ictus…) o derivada de la progresión retrógrada donde produce hemopericardio y taponamiento cardíaco. Actualmente, la angio Tomografía Computerizada (angioTC) y la Ecocardiografía Transesofágica (ETE) son las pruebas diagnósticas más utilizadas, presentando una sensibilidad y especificidad cercana al 100% en ambas pruebas5
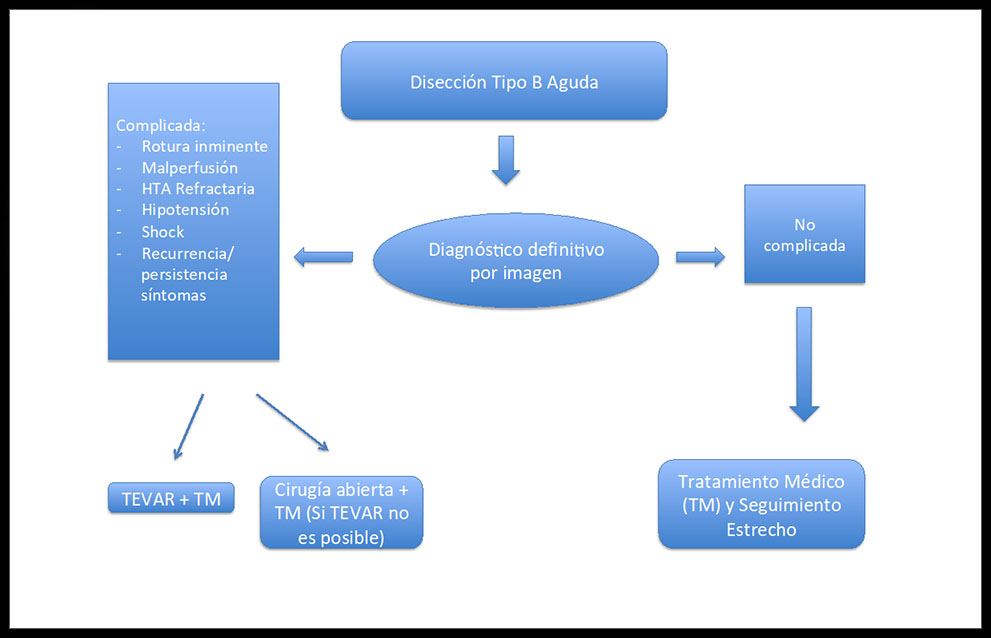
En cuanto al tratamiento, en la figura 1 viene representado un esquema básico del tratamiento de esta enfermedad. No obstante, hay evidencia de que la trombosis de la LF y la remodelación aórtica aporta beneficios a largo plazo6, de manera que a 5 años la mortalidad es menor en pacientes intervenidos sometidos a reparación endovascular (TEVAR) que en pacientes tratados médicamente7. Así, se han identificado una serie de predictores clínicos (edad joven, sexo masculino, raza caucásica…) y radiológicos (diámetro aórtico mayor de 40 mm al inicio, trombosis parcial de la LF, desgarro aórtico único…) que asocian mayor crecimiento aórtico y mayor mortalidad8. Por tanto, debemos individualizar el tratamiento en función de las características de cada paciente.
Figura 1: Algoritmo terapéutico en la Disección tipo B
CASO CLÍNICO
Paciente de 39 años que acude al Servicio de Urgencias de nuestro centro por episodio de dolor centrotorácico brusco de dos horas de duración asociado a mal control tensional. Como antecedentes destacan:
- Hipertensión Arterial.
- Hipertrofia ventricular secundaria a miocardiopatía hipertensiva con función sistólica conservada. Sin anomalías del arco aórtico.
- Hábitos tóxicos: Tabaquismo activo. Consumidor ocasional de marihuana.
El paciente es diagnosticado de disección aórtica tipo B según la clasificación de Stanford que se extiende a aorta abdominal. La Arteria Renal derecha nace de LF. En el TAC también se identifican lesiones isquémicas en el riñón derecho. No obstante, no presenta deterioro de la función renal en la analítica.
Es intervenido de forma urgente mediante técnica Petticoat: se le colocaron 2 endoprótesis torácicas Gore TAG enrasadas distal al origen de la Arteria Subclavia izquierda; y 2 Stent no recubiertos E-XL en aorta visceral. Además, se le colocó un Stent Balón Expandible en Arteria Iliaca Común derecha por disección residual. Se consigue trombosis de la LF que se confirma mediante ETE intraoperatoria pero se objetiva trombosis de la Arteria Renal derecha que emergía del falso lumen. Se intentó intraoperatoriamente recanalizar dicha arteria pero no se consiguió. El paciente fue dado de alta a los 4 días sin deterioro de función renal y con buen control tensional.
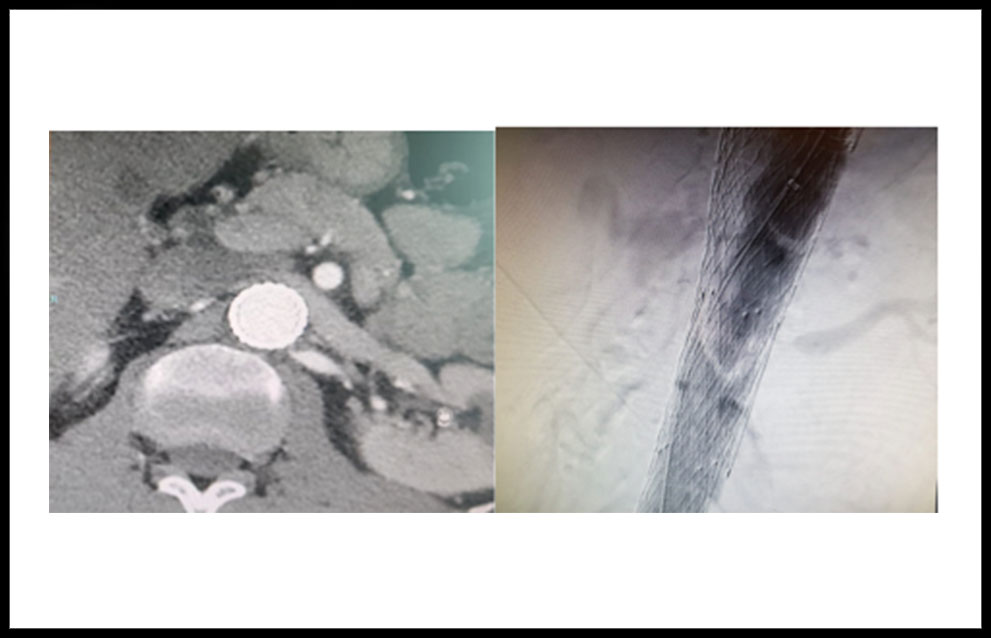
Al año de seguimiento, el paciente comienza a referir clínica de varios meses de evolución de ortopnea, mayor por la noche, e hipertensión, acompañado de aumento de la creatinina sérica. En el AngioTC se identifica una estenosis crítica en el origen de la Arteria Renal izquierda que podemos observar en la Figura 2.
Figura 2: Estenosis crítica en origen de arteria renal izquierda
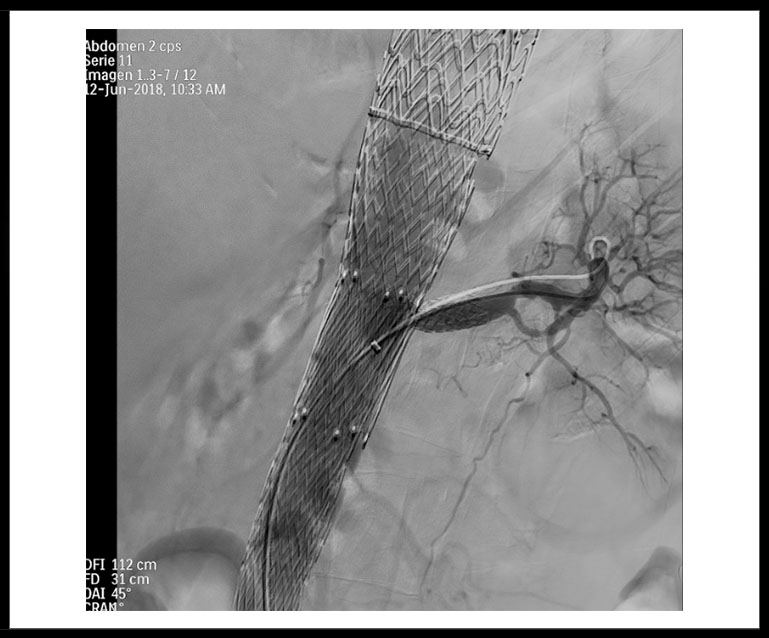
Ante tales hallazgos, decidimos intervenir al paciente. Se realiza la colocación, mediante acceso percutáneo femoral izquierdo, de un Stent Balón-Expandible en la Arteria Renal izquierda a través del Stent E-XL, con predilatación progresiva de dicho Stent con 2 balones de alta presión de diámetro creciente. En la Figura 3, podemos ver el resultado arteriográfico final tras la colocación del Stent.
Figura 3: Control arteriográfico final tras la implantación del stent
El paciente fue dado de alta al día siguiente sin complicaciones del sitio de punción y con mejoría de la función renal. A los 6 meses continúa sin clínica de Insuficiencia Cardíaca y sin deterioro de la función renal.
DISCUSIÓN
El tratamiento óptimo de la disección tipo B incluye un diagnóstico precoz, un rápido control de la tensión arterial y un pronto reconocimiento del síndrome de malperfusión o cualquiera de sus otras posibles complicaciones.
El tratamiento clásico de la disección tipo B consistía principalmente en el manejo médico de la misma pues presenta mejores tasas de mortalidad que la reparación abierta y endovascular. Sin embargo, la consecuencia tardía de la terapia médica consiste en la degeneración aneurismática de la LF que puede llegar a ocurrir hasta en el 40% de los pacientes. De hecho, en algunas series, la terapia médica falló a largo plazo hasta en el 58% de los pacientes pues un 29% de los mismos precisó cirugía (generalmente para la reparación de degeneraciones aneurismáticas) y un 38% fallecieron, con un seguimiento medio de 4,3 años9.
Así, la historia natural de los pacientes tratados médicamente sugiere que hay un subgrupo de pacientes que se benefician de la terapia endovascular en el período subagudo tras la aparición de los síntomas. Con la cobertura del desgarro principal, inducimos la trombosis de la falsa luz y con ello, se reduce el riesgo de degeneración aneurismática posterior.
De ahí la importancia del seguimiento de estos pacientes, dado que el remodelado aórtico tras el tratamiento endovascular de la disección constituye un proceso dinámico que requiere un seguimiento para controlar el diámetro aórtico y posibles alteraciones de los troncos viscerales.
Por otro lado, la terapia endovascular parece ser la más idónea en la resolución de los procedimientos endovasculares complejos pues disminuye y minimiza la morbimortalidad de una reparación quirúrgica clásica. Podemos decir que una terapia endovascular precoz para esta patología, especialmente cuando se trata de un síndrome de malperfusión propiamente dicho, ha demostrado disminuir las tasas de mortalidad10.
REFERENCIAS BIBLIOGRÁFICAS
- Khan IA, et al. Clinical, diagnostic and management perspectives of aortic dissection. Chest. 122: 311-328, 2002.
- Clouse WD; Hallet Jr JW; Schaff HV, et al. Acude aortic dissection: population-based incidence compared with degenerative aortic aneurysm rupture. Mayo Clin Proc. 79:176-180 2004.
- Daily PO; Trueblood H; Stinson EB. Management of acute aortic dissection. Ann Thorac Surg. 10:237-246 1970.
- Desai ND; Gottret JP; Szeto WY; et al. Impact of timing on major complicacions after thoracic endovascular aortic repair for acute type B aortic dissection. J Thorac Cardiovasc Surg. 149:S151-S156 2015.
- Fisher ER, Stern EJ, Godwin 2nd JD; Otto CM; Johnson JA. Acute aortic dissection: typical and atypical imaging features. Radiographics. 14: 1263-1271 1994
- Akin I; Kische S; Ince H; et al. Indication, timing and results of endorvascular treatment of type B dissection. Eur J Vasc Endovasc Surg 37: 289-96, 2009.
- Ulug P; McCaslin JE; Stansby G; et al. Endovascular versus conventional medical treatment for uncomplicated chronic type B aortic dissection. Cochrane Database Syst Rev 11: CD006512. 2012.
- Nienaber CA; Kische S; Rousseau H; Eggebrecht H; Rehders TC; Kundt G; et al. Endovascular repair of type B aortic dissection: long-term results of the randomized investigation of stent grafts in aortic dissection trial. INSTEAD-XL trial. Circ Cardiovasc Interv 6(4): 407-16, 2013.
- Durham CA; Cambria RP; Wang LJ; et al. The natural history of medically managed acute type B aortic dissection. J Vasc Surg. 61:1192-1198 2015
- Bernes DM, Williams DM; Dasika NL; et al. A single-center experience treating renal malperfusion after aortic dissection with central aortic fenestration and renal artery stenting. J Vasc Surg. 2008 May; 47(5): 903-910
INFORMACIÓN DEL ARTÍCULO
Autor para la correspondencia: J.A. Fernández Herrera. Unidad de Gestión Clínica de Angiología y Cirugía. Vascular del Hospital Universitario San Cecilio de Granada. Avenida de la Innovación S/N. Código Postal 18016