Original
Caracterización de Agarosas Tipo I y Tipo VII para su uso en Ingeniería Tisular
Type I and type VII agarose characterization for use in tissue engineering
Actual. Med. 2017; 102: (802): 145-150 DOI: 10.15568/am.2017.802.or03
Enviado: 26-11-2017
Revisado: 28-11-2017
Aceptado: 16-12-2017
RESUMEN
Objetivos: El objetivo del presente trabajo es el desarrollo de un nuevo protocolo para la inclusión de geles de agarosa en parafina que permita su estudio en histología, y la posterior caracterización de dos tipos distintos de agarosa, Tipo I y Tipo VII, para su uso en Ingeniería Tisular.
Material y métodos: Se evaluaron distintos protocolos que permitiesen un correcto procesamiento de los geles de agarosa permitiendo obtener cortes de dichos geles incluidos en parafina. Una vez optimizado el protocolo, se realizó una caracterización de las agarosas tipo I y VII para su utilización en Ingeniería Tisular. Para ello se obtuvieron geles de agarosa de ambos tipos a concentraciones del 2% y 2.5%, y en cuyo interior había condrocitos. Se evaluó la permeabilidad de la membrana celular mediante la medida por espectrofotometría del ADN liberado al medio, el tamaño celular de los condrocitos cultivados y el estado celular mediante inmunohistoquímica frente a PCNA y Vimentina. También se realizó un estudio sobre la resistencia a la compresión que presentan los distintos geles con el paso del tiempo.
Resultados: Tres de los protocolos propuestos hacían posible el procesamiento de los geles y permitieron la caracterización de los distintos tipos de agarosa. En este caso, el estudio de las agarosas tipo I y VII ha demostrado que los condrocitos crecen correctamente en ambos tipos de agarosas, pero que la tipo VII favorece el desarrollo de los mismos frente a la Tipo I. Además, la agarosa pierde elasticidad con el paso de los días soportando a la vez menos fuerza de compresión.
Conclusiones: El Protocolo propuesto para el procesamiento y posterior inclusión de geles de agarosa en parafina en este trabajo permite realizar histología en los mismos, y ha permitido confirmar que la agarosa tipo VII favorece el desarrollo y supervivencia celular.
Palabras clave: agarosa, gel, condrocito, Ingeniería Tisular.
ABSTRACT
Introduction: The objective of the present work is the development of a new protocol for the inclusion of paraffin-embedded agarose gels to allow their study in histology and the subsequent characterization of two different types of agarose, Type I and Type VII, for their use in Tissue Engineering.
Materials y methods: Different protocols were evaluated for a correct processing of the agarose gels allowing to obtain cuts of paraffin-embedded agarose gels. Once the protocol was optimized, a characterization of type I and VII agarose was performed for their use in tissue engineering. For this purpose, agarose gels of both types were obtained at concentrations of 2% and 2.5%, and in which chondrocytes were present. The permeability of the nuclear membrane was measured by spectrophotometry of the DNA released, the cell size of the cultured chondrocytes and the cellular state by immunohistochemistry against PCNA and Vimentin. A study on the compressive strength of different gels over time was also performed.
Results: Three of the proposed protocols allowed the processing of the gels and allowed the characterization of the different types of agarose. In this case, the study of the type I and VII agarose has shown that chondrocytes grow correctly in both types of agarose, but type VII favors the development of the same against Type I. In addition, the agarose loses elasticity with the day pass while supporting less compressive force.
Conclusions: The proposed protocol for the processing and subsequent inclusion of paraffin-agarose gels in this work allows the histology to be carried out in the same ones, and has allowed to confirm that type VII agarose favors the development and cellular survival.
Keywords: agarose, gel, chondrocyte, Tissue Engineering
Leer Artículo Completo
INTRODUCCIÓN
La Ingeniería Tisular es una ciencia multidisciplinaria cuyo objetivo es el desarrollo de estrategias para la generación de órganos y tejidos completamente funcionales; estrategias que se basan en la interacción de tres componentes fundamentales como son: células, factores de crecimiento y andamios (1).
La función del andamio es servir como soporte estructural y guía para la formación del nuevo tejido, proporcionando un ambiente en tres dimensiones, que facilite la adherencia, migración, proliferación y organización espacial tridimensional de las células, y por tanto juega un papel determinante en el crecimiento y diferenciación celular (2). Alguno de los andamios utilizados en Ingeniería Tisular son colágeno, fibrina y distintos tipos de polímeros naturales, ya que presentan propiedades similares a las de la matriz extracelular nativa (3). Estos biomateriales pueden extraerse de plantas, animales, algas o pueden ser sintetizados por microorganismos (4).
La agarosa es un polisacárido procedente de las algas marinas que tiene la capacidad de formar geles térmicamente reversibles (5). Estructuralmente es un polímero lineal que consiste en unidades alternas de D-galactosa y 3,6-anhidro-L-galactosa. Este polisacárido es soluble en agua a temperaturas por encima de 65ºC y, dependiendo del grado de sustituciones de hidroxietilo en sus cadenas laterales, gelifica en un rango de temperaturas comprendido entre 17-40ºC (6), dando lugar a distintos tipos de agarosas comerciales. Una vez que los geles de agarosa son estables no se vuelven a hacer líquidos hasta alcanzar temperaturas mayores a 65ºC. Esta característica en la que las temperaturas de fusión y gelificación son distintas recibe el nombre de histéresis térmica (7).
Entre sus múltiples usos destaca su utilización para la obtención de geles para el cultivo de células en Ingeniería Tisular (8). La estructura física de dichos geles puede ser controlada usando distintas concentraciones de agarosa, lo que da lugar a diversos tamaños de poro. Los grandes poros y la baja rigidez mecánica de los geles a bajas concentraciones de agarosa pueden permitir la migración y proliferación de células (9). Entre sus aplicaciones en Ingeniería Tisular destaca su uso conjugado con fibrina para la obtención de hidrogeles de fibrina-agarosa que permiten la elaboración de tejidos artificiales como piel (10), córnea (11), mucosa oral (12) y nervio (13). Por otro lado, los geles de agarosa suelen también utilizarse, en Ingeniería Tisular, para la reparación del cartílago (14), ya que favorecen el crecimiento y la diferenciación de los condrocitos (15).
Uno de los procedimientos más usados en histología es la inclusión en parafina de las muestras, ya que permite su conservación sin la necesidad de poseer un equipo que las mantenga (16). Sin embargo, las características de la agarosa, sobre todo su baja temperatura de fusión, hace muy difícil el procesamiento de los constructos fabricados con este material para su estudio en histología. Por ello se hace necesario establecer una nueva metodología que permita el procesamiento de los geles de agarosa para su estudio. El objetivo del presente trabajo consiste en desarrollar un nuevo protocolo para la inclusión de geles de agarosa en parafina y, por otro lado, la caracterización de dos tipos distintos de agarosa, Tipo I y Tipo VII, para su uso en Ingeniería Tisular.
MATERIALES Y MÉTODOS
2.1. Protocolo Procesamiento de Geles de Agarosa
a.Elaboración de los geles
Para la elaboración de los geles se partió de agarosa tipo VII al 2% (Sigma – Aldrich, Steinheim, Alemania) preparada en Solución Tamponada con Fosfato (PBS) (Sigma-Aldrich). La agarosa fue calentada hasta hacerse líquida y se distribuyó en placas de Petri de 55mm. Una vez gelificado, se obtuvieron punchs de 8 mm del gel.
b.Evaluación de los protocolos
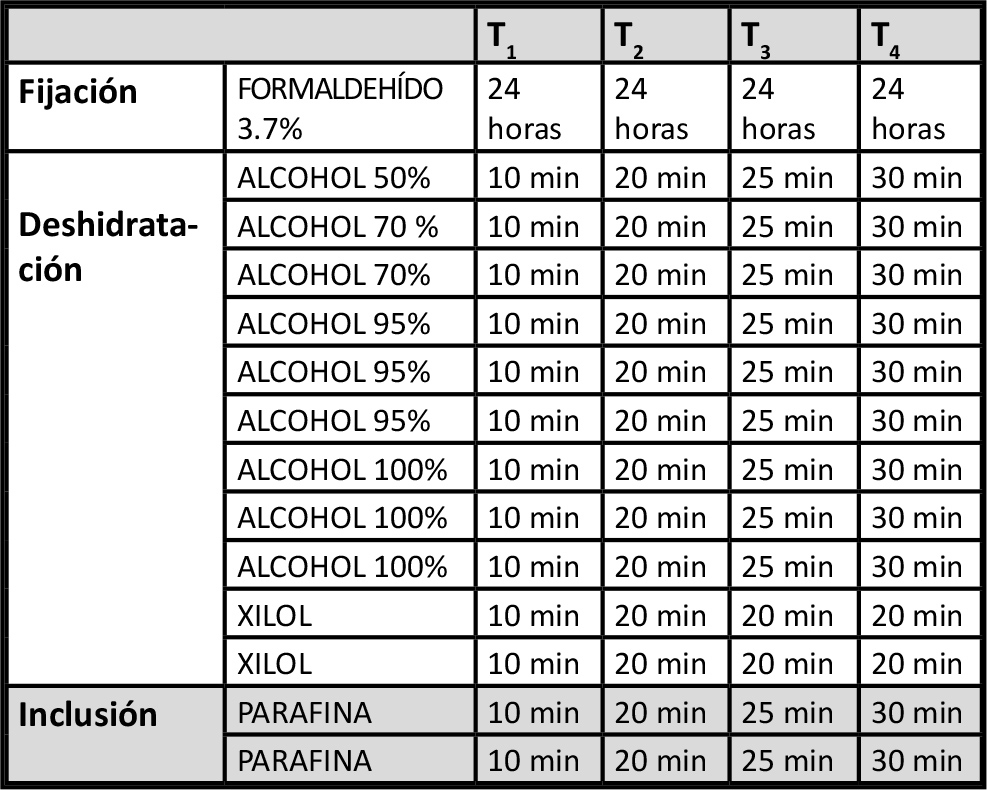
Una vez obtenidos los geles, fueron procesados de acuerdo a cuatro protocolos, basados en la metodología habitual de procesamiento para inclusión en parafina (17), y que se diferencian en el tiempo de deshidratación e inclusión (Tabla 1). Tras la inclusión en parafina, se obtuvieron cortes de 5 µm que fueron teñidos con Hematoxilina-Eosina para poder determinar cuál era el procedimiento idóneo.
Tabla 1. Tabla 1. Protocolos para el Procesamiento de Geles de Agarosa. (8)
2.2.Caracterización de Agarosa Tipo I y Tipo VII
a.Cultivo de Condrocitos
Los condrocitos se obtuvieron a partir de biopsias de tejido cartilaginoso de rata. Las muestras fueron fragmentadas mecánicamente en pequeños trozos e incubadas a 37.5ºC en una solución estéril de colagenasa tipo I de Clostridium hystoliticum (Gibco BRL Life Technologies Ref. 17100-017, Karlsruhe, Alemania) al 2% en medio de cultivo DMEM durante 7 horas. Posteriormente los condrocitos fueron aislados mediante centrifugación y cultivados en medio de expansión para condrocitos [DMEM-F12 (GIBCO) suplementado con Suero Fetal Bovino al 10% (FBS, Sigma-Aldrich), Solución Antibiótica al 1% (100 U/ml de penicilina G, 100 μg/ml Estreptomicina y 0,25 μg/ml de anfotericina B, Sigma – Aldrich, Steinheim, Alemania) y 2mM de L-glutamina (Sigma-Aldrich, Alemania)] a 37.5ºC y 5% de dióxido de carbono. El medio de cultivo se renovó cada 3 días y los condrocitos se expandieron hasta el pase VI para su utilización en la elaboración de los constructos.
b.Fabricación de los geles
Los geles de agarosa se elaboraron utilizando dos tipos distintos: Agarosa Tipo I y Tipo VII (Sigma-Aldrich). La agarosa Tipo I es un tipo de agarosa comercial cuya temperatura de gelificación está comprendida entre los 34.5-37.5ºC, mientras que la agarosa Tipo VII o Agarosa Low Gelling Temperature, se caracteriza por tener una temperatura de gelificación que oscila entre los 24-28ºC. En Ingeniería Tisular la agarosa normalmente utilizada para la elaboración de constructos es de tipo VII ya que su baja temperatura de gelificación permite que las células no disminuyan su viabilidad. En este caso, para caracterizar ambos tipos de agarosa y determinar la viabilidad celular en cada una de las condiciones anteriormente citadas, se fabricaron geles a dos concentraciones, 2% y 2.5%, partiendo de agarosa estéril al 4% preparada en Solución Tamponada con Fosfato (PBS) (Sigma-Aldrich). Para ello se prepararon 3 mL de mezcla para cada condición que contenía agarosa estéril líquida al 4%, y condrocitos en medio condrogénico [DMEM-F12 (GIBCO) suplementado con Solución Antibiótica al 0.1%, 2mM de Piruvato de sodio (GIBCO), ITS al 0.1%, 4 µM de Ácido ascórbico (Sigma – Aldrich), 10 ng/mL de TGF-β1, 10 µM de Dexametasona (Sigma – Aldrich) y 0.35 mM de L-Prolina (Sigma-Aldrich)]. Tras homogeneizar cuidadosamente, esta mezcla se distribuyó en placas de 12 pocillos (3 pocillos por condición) en alícuotas de 1 mL que contenían 100.000 células. Una vez gelificado, se le añadió medio condrogénico para favorecer el desarrollo de los condrocitos y este se renovó cada 2 días. Se realizaron 3 placas exactamente iguales para realizar los estudios a los 2, 8 y 16 días. Las placas se mantuvieron en un ambiente de 37.5ºC y 5% de CO2.
c.Liberación de ADN
Una forma de estudiar la muerte celular es mediante la evaluación de la permeabilidad de la membrana celular. El ADN liberado se cuantificó en un espectrofotómetro UV-Vis NanoDrop 2000 (Thermo Fisher Scientific) por espectrofotometría a λ = 260-280 nm, siguiendo el método descrito previamente por Rodríguez-Arco (18). El sobrenadante del medio de cultivo se colocó en tubos Eppendorf para la cuantificación de ADN. Para este análisis se utilizaron tres geles de cada modalidad y se registraron tres determinaciones para cada uno (n = 9 para cada condición). Como control negativo las células fueron tratadas con Triton X-100 al 2% durante 10 minutos, introduciéndose una liberación elevada de ADN debido al daño irreversible en las membranas plasmáticas y nucleares. Se utilizó agua destilada y medio de cultivo como controles para la técnica de ensayo.
d.Evaluación Histológica
Para los análisis histológicos e inmunohistoquímicos, los geles fueron procesados utilizando el Protocolo T3 descrito con anterioridad. Una vez que los geles fueron incluidos en parafina, se obtuvieron secciones transversales de 5 μm de cada uno de ellos. Los cortes se tiñeron con azul Alcian y se contrastaron con Nuclean Fast Red (19) para su observación al microscopio y obtener el área celular. Para estudiar el comportamiento celular, se analizaron diferentes procesos celulares mediante técnicas inmunohistoquímicas (13). Se utilizó el antígeno nuclear de células en proliferación (PCNA) para identificar las células proliferantes (20). También, se utilizó el anticuerpo frente a la Vimentina para identificar aquellas células que mantenían la integridad física (21). Para cada reacción inmunohistoquímica, se utilizaron controles para asegurar el correcto funcionamiento de los anticuerpos. Todos los procedimientos se realizaron bajo las mismas condiciones para asegurar la reproducibilidad de los resultados.
e.Estudios de compresión
Para realizar los estudios de compresión de los distintos geles se utilizó un sistema electromecánico para ensayos de materiales Instron, Modelo 3345-53327. Se utilizaron geles sin células de ambos tipos de agarosas a concentraciones del 2% y 2.5% para realizar las medidas. Para obtener resultados fiables, la compresión se realizó suavemente de modo que la fuerza normal que actuaba sobre la muestra era siempre inferior a 0.05 N y la separación placa-placa era de 3 mm. El módulo de Young (E) se calculó como la tangente de la porción lineal inicial de la curva esfuerzo-deformación de cada prueba experimental, mientras que los valores del esfuerzo a rotura (σ) y de la deformación a rotura (ε) se determinaron mediante la selección del punto de la curva de esfuerzo-deformación donde se produjo la fractura.
f.Tratamiento estadístico
Los datos obtenidos se analizaron, para la presencia de valores atípicos, usando el test de Grubb (método ESD). Los análisis estadísticos se llevaron a cabo utilizando el programa informático Statgraphics Centurion XVI v.16.1.03 mediante ANOVA Simple. Seguidamente, se realizó un test de Tukey para la comparación entre grupos significativamente diferentes, siendo considerados estadísticamente diferentes cuando p<0.05.
RESULTADOS
3.1. Protocolo Procesamiento de Geles de Agarosa
Los geles de agarosa procesados mediante los protocolos T2, T3 y T4 nos permitieron obtener cortes de los mismos tras la inclusión en parafina, a diferencia de los geles sometidos al protocolo T1. En estos últimos, los geles incluidos en parafina presentaron cierta dureza que impedía el corte de los mismos. Con microscopía óptica se observó una estructura fibrilar tanto en T2 como en T3, y que estaba ausente en T4. (Figura 1)
Figura 1. Imágenes obtenidas por microscopía de los cortes de los geles a los que se les realizó los protocolos de procesamiento T2, T3 y T4 a los aumentos 4x y 40x.
3.2 Caracterización de Agarosa Tipo I y Tipo VII
a. Liberación de ADN
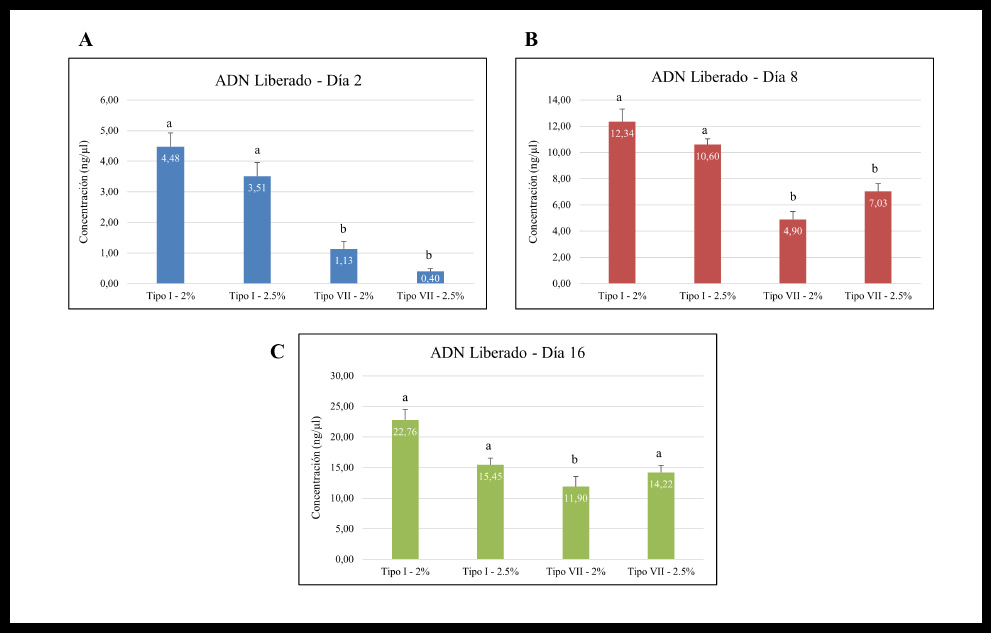
El análisis por espectrofotometría de la liberación de ADN (Figura 2), como resultado del daño irreversible en la membrana celular, pone de relieve que la liberación de ADN es mayor en los geles de agarosa Tipo I en relación con la agarosa Tipo VII al 2% y 2.5%, respectivamente, a los 2, 8 y 16 días de cultivo. Mediante el tratamiento estadístico de los resultados se observó que existía una diferencia estadísticamente significativa de la liberación de ADN entre las distintas condiciones de cultivo (Tipo de agarosa y concentración) con un nivel del 95.0% de confianza. Para los días 2 y 8, mediante el Test de Tuckey, se distinguieron dos grupos homogéneos correspondientes a cada tipo de agarosa independientemente de la concentración utilizada. Mientras que para el día 16 dicho test estableció dos grupos homogéneos, uno formado por la agarosa tipo I y la condición agarosa tipo VII al 2.5%, y otro por la condición agarosa tipo VII al 2%.
b. Evaluación Histológica
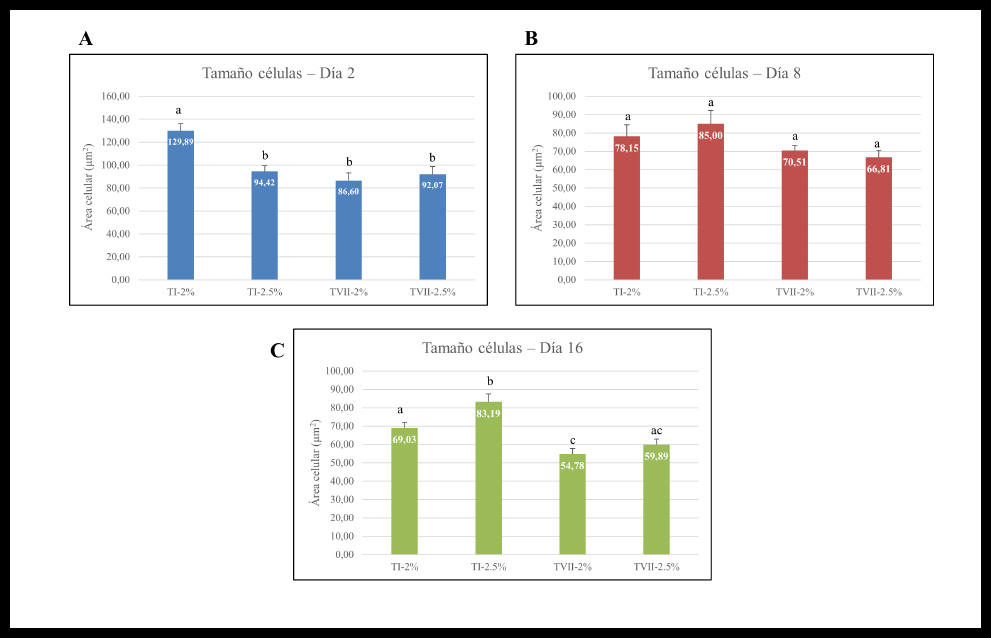
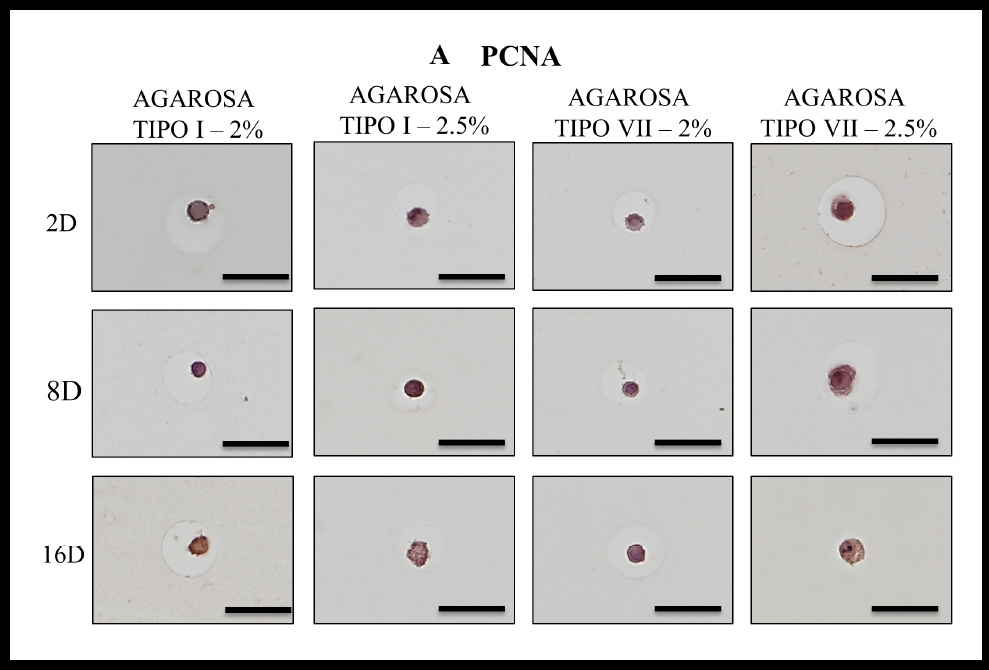
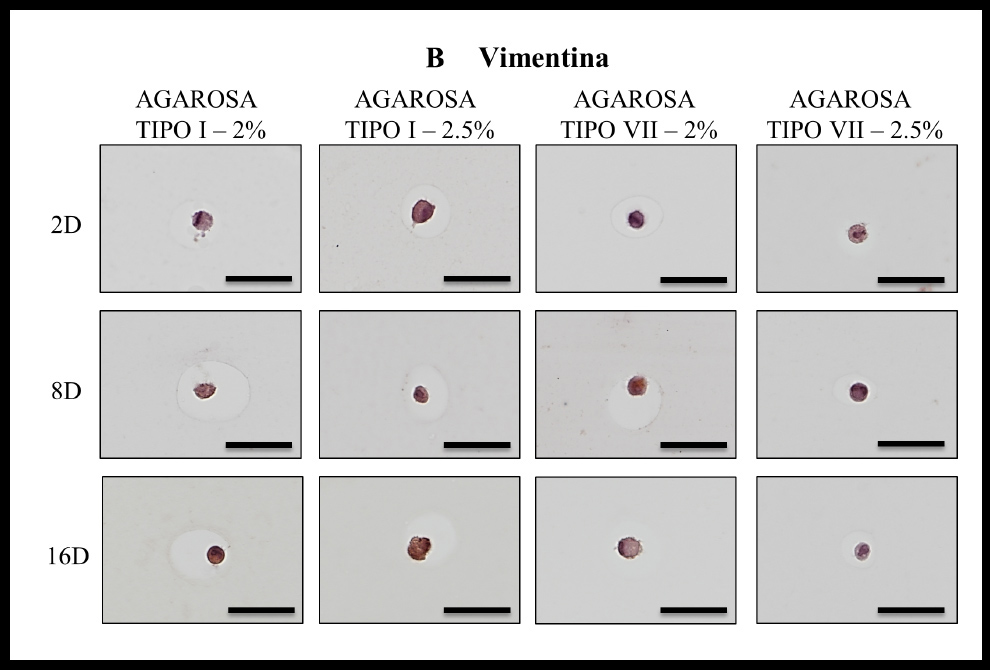
El análisis del área celular, en cada una de las condiciones y en los distintos tiempos, puso de relieve en el día 2 diferencias estadísticamente significativas entre el tamaño y las condiciones de cultivo, identificándose dos grupos (Figura 4, A), uno formado por la agarosa Tipo I al 2% donde el tamaño es superior, y otro grupo formado por las condiciones restantes. En el día 8 (Figura 4, B) no existían diferencias estadísticamente significativas entre el tamaño y las condiciones de cultivo, identificándose un solo grupo homogéneo. Mientras que en el día 16 (Figura 4, C) sí existían diferencias estadísticamente significativas entre el tamaño y las condiciones de cultivo, identificándose tres grupos homogéneos. El test de Tuckey estableció que la agarosa tipo VII al 2% formaba parte tanto del grupo “Agarosa tipo VII al 2.5%” como del grupo “Agarosa tipo I al 2%.” A Los resultados obtenidos de los análisis inmunohistoquímicos resultaron ser positivos tanto para PCNA (Figura 3, A) como Vimentina (Figura 3, B).
Figura 2. Representación gráfica del ensayo de liberación de ADN. Liberación de ADN Día 2 (A), Día 8 (B) y Día 16 (C). Quedan representados los niveles de liberación de ADN (ng/μL) respecto a las distintas condiciones de cultivo. Los gráficos representan la media ± SEM (n=9). Las letras simbolizan grupos con diferencias estadísticamente significativas para cada Tratamiento (ANOVA a una vía, p < 0,05). El control negativo poseía un valor medio de 246.33 ng/μL.
Figura 4. Representación gráfica del ensayo de tamaño celular. Día 2 (D), Día 8 (E) y Día 16 (F) quedan representados el área celular (μm2) respecto a las distintas condiciones de cultivo. Los gráficos representan la media ± SEM (n=10). Las letras simbolizan grupos con diferencias estadísticamente significativas para cada Tratamiento (ANOVA a una vía, p < 0,05).
Figura 3 A. Resultados Inmunohistoquímica PCNA (A) y Vimentina (B).
Figura 3 B. Resultados Inmunohistoquímica PCNA (A) y Vimentina (B).
c. Estudios de compresión
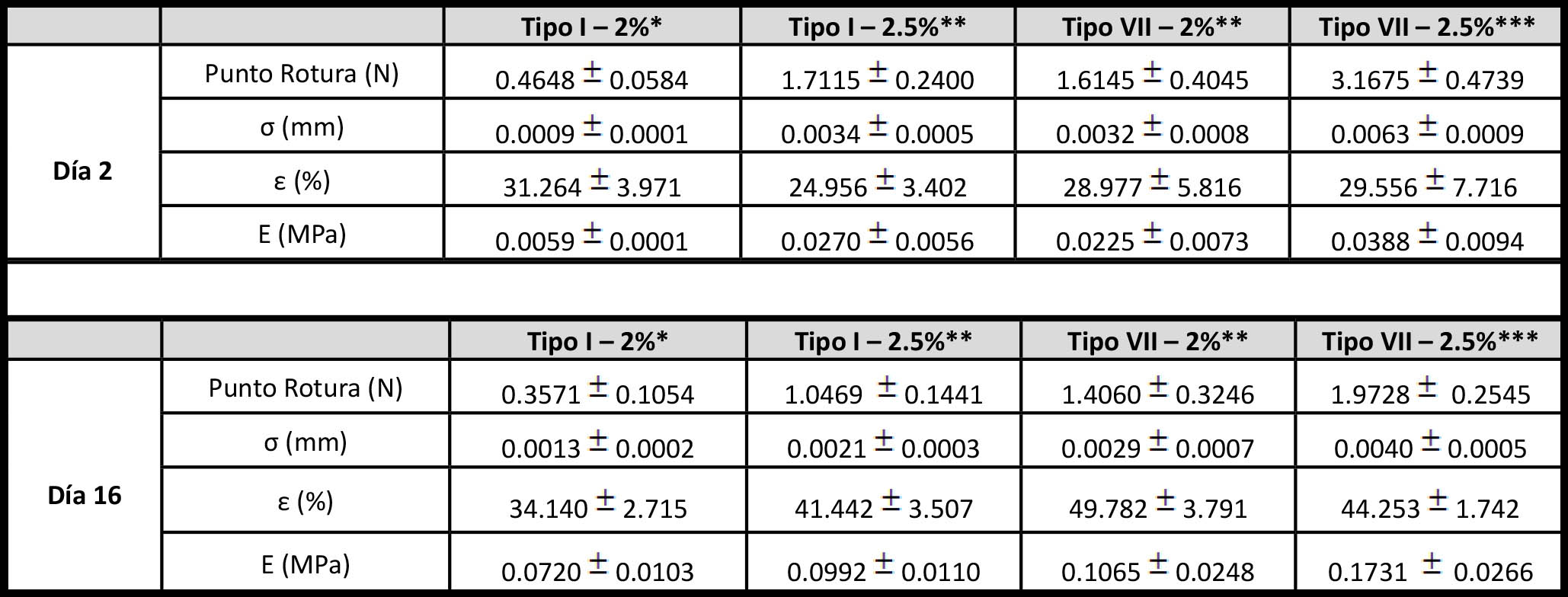
Tras la realización de los estudios de compresión se obtuvo el módulo de Young o módulo de elasticidad y la Fuerza en el punto de rotura para cada una de las condiciones (Tabla 2). Como se puede observar el módulo de Young es más pequeño en los geles del día 2 que en los del día 16, lo que indica que los geles con el paso del tiempo van perdiendo elasticidad y volviéndose más rígidos, además alcanzan el punto de rotura a una compresión menor que sus homólogos en días anteriores. Es necesario destacar, que los geles de agarosa Tipo I – 2.5% y Tipo VII – 2% presentan comportamientos similares. La agarosa Tipo I – 2% por su parte presenta mayor elasticidad pero resiste menos fuerza que las otras condiciones, mientras que al Tipo VII – 2.5% le ocurre justamente lo contrario, tiene un menor módulo de elasticidad pero resiste más fuerza. Tras el análisis estadístico de los datos se observó que existían diferencias estadísticamente significativas entre las distintas condiciones. Mediante el test de Tuckey, se identificaron tres grupos homogéneos donde la condición Tipo I – 2.5% y la Tipo VII – 2% formaban parte del mismo grupo. Asimismo existían diferencias estadísticamente significativas entre el día 2 y 16 para cada una de las condiciones.
Tabla 2. Resultados obtenidos de las pruebas de compresión realizadas. Se representan la media ± Desviación Estándar (n=10) del Punto de Rotura, esfuerzo a rotura (σ), deformación a rotura (ε) y el módulo de Young (E). Las asteriscos (*) simbolizan grupos con diferencias estadísticamente significativas para cada condición (ANOVA a una vía, p < 0,05).
DISCUSIÓN
Establecer un protocolo que permita el procesamiento y la posterior inclusión de geles de agarosa en parafina contribuye al estudio de este tipo de geles, y por tanto, a su desarrollo y a la posibilidad de que en un futuro se extienda el uso de este biomaterial en biomedicina. Los resultados obtenidos en este trabajo demostraron que los protocolos T2, T3 y T4 permitían obtener cortes al micrótomo y posteriormente realizar análisis histológicos. En este caso se decidió utilizar T3 porque sus tiempos eran intermedios con respecto a los otros dos protocolos, dándonos un margen de 5 minutos en cada uno de los pasos de deshidratación e inclusión. Además como se puede observar en la Figura 1, en los cortes obtenidos por T3 se distingue la estructura fibrilar de los geles de agarosa (22), lo que indica que el gel sigue manteniendo su estructura tras el procesamiento.
En cuanto a la caracterización de los distintos tipos de agarosa, los estudios de integridad de la membrana celular, por la medida de la liberación del ADN al medio, mostraron que las células cultivadas en agarosa tipo VII liberan menor cantidad de ADN que las cultivadas en agarosa tipo I. Esto revela que las células cultivadas en agarosa tipo VII presentan mayor viabilidad que las cultivadas en agarosa tipo I. Además, existen diferencias estadísticamente significativas entre ambos tipos de agarosas, mientras que la concentración de agarosa parece no afectar en gran medida a la viabilidad celular. De manera que podemos establecer que la viabilidad de los condrocitos se ve afectada principalmente por el tipo de agarosa utilizada para su cultivo. Esto se puede deber, principalmente, al hecho de que a la hora de elaborar el constructo la agarosa tipo I necesita una temperatura algo mayor a los 35ºC para mantenerse líquida y poder obtener el gel con las células en su interior, lo que puede afectar a la integridad de la célula y puede favorecer a una muerte prematura de la misma.
Por otro lado, el tamaño celular que presentan los condrocitos se ve más afectado con el paso del tiempo que con el tipo de agarosa y la concentración utilizada, aunque aparezcan pequeñas diferencias en días más tempranos.
Se puede observar que en el día 8 de cultivo todos los condrocitos presentan aproximadamente un tamaño similar independientemente de la condición de cultivo. Es en el día 16 cuando ya aparecen más diferencias, las cuales se pueden deber principalmente al tiempo en cultivo y a la degradación que va sufriendo la agarosa, la cual se va deshidratando, lo que explicaría la disminución del tamaño celular. Por lo tanto, el tamaño celular no se ve afectado por la condición de cultivo, sin embargo, la degradación que sufre la agarosa en el tiempo hace que disminuya el tamaño celular y que aparezcan diferencias en el mismo.
Por otra parte, el resultado de los análisis inmunohistoquímicos realizados pone de relieve que los condrocitos son viables y que presentan una estructura adecuada durante el tiempo de estudio, independientemente del tipo de agarosa y la concentración utilizada, lo que deja claro que la agarosa favorece el crecimiento de los condrocitos en cultivo.
En cuanto al estudio de compresión de los Geles, ha demostrado que el paso del tiempo hace que el módulo de Young o módulo de elasticidad de los geles aumente, lo que se traduce en un aumento de la rigidez. Este aumento de la rigidez hace que los geles sean más frágiles y disminuyan su resistencia a la compresión. Este efecto se puede explicar por la degradación que sufre la agarosa con el paso del tiempo (23). Por otro lado, los geles de agarosa tipo I presentan menor resistencia a la compresión que los geles de agarosa tipo VII a la misma concentración. Asimismo, los geles de agarosa a concentraciones del 2% presentan menor resistencia a la compresión que los geles a una concentración del 2.5%. Sin embargo, es importante destacar que el estudio pone de relieve que la agarosa tipo I al 2.5% presenta un comportamiento reológico similar a la tipo VII al 2%. En este caso, sería importante tener en cuenta las características biomecánicas del tejido humano que se quiere obtener por Ingeniería Tisular.
CONCLUSIÓN
El Protocolo propuesto para el procesamiento y posterior inclusión de geles de agarosa en parafina en este trabajo permite realizar el análisis histológico de los mismos, haciendo posible en este caso la caracterización de la agarosa tipo I y tipo VII.
En el presente trabajo se ha podido comprobar que los condrocitos crecen en ambos tipos de agarosa. Sin embargo, se ha podido observar que la agarosa tipo VII favorece el desarrollo y supervivencia celular durante el tiempo de estudio frente a la agarosa tipo I. Las investigaciones realizadas en este campo permitirán, por tanto, el abrir nuevas vías de trabajo en la regeneración de cartílago.
REFERENCIAS
- Nerem RM, Sambanis A. Tissue Engineering: From Biology to Biological Substitutes. Tissue Eng. 1995;1(1):3–13.
- O’Brien FJ. Biomaterials & scaffolds for tissue engineering. Mater Today. 2011;14(3):88–95.
- Patel H, Bonde M, Srinivasan G. Biomedical Applications of Hydrogels Handbook. Ottenbrite RM, Park K, Okano T, editors. Vol. 25, Trends Biomater. Artif. Organs. New York, NY: Springer New York; 2010. 20-29 p.
- Santos Estévez L. Síntesis y caracterización de scaffolds poliméricos para la ingeniería de tejidos. Tesis Doctoral. Universidad de Valencia; 2013.
- Jin R, Dijkstra PJ. Hydrogels for Tissue Engineering Applications. Biomed Appl Hydrogels Handb. 2010;101(7):203–25.
- Shillito RD, Paszkowski J, Potrykus I. Agarose Plating and a Bead Type Culture Technique Enable and Stimulate Development of Protplast-Derived Colonies in a Number of Plant Species. Plant Cell Rep. 1989;2:304–7.
- Balgude AP, Yu X, Szymanski A, Bellamkonda R V. Agarose gel stiffness determines rate of DRG neurite extension in 3D cultures. Biomaterials. 2001;22(10):1077–84.
- Kessler MW, Grande DA. Tissue engineering and cartilage. Organogenesis. 2008;4(1):28–32.
- Dillon GP, Yu X, Sridharan A, Ranieri JP, Bellamkonda R V. The influence of physical structure and charge on neurite extension in a 3D hydrogel scaffold. J Biomater Sci Polym Ed. 1998;9(10):1049–69.
- Carriel V, Garzon I, Jimrnez JM, Oliveira ACX, Arias-Santiago S, Campos A, et al. Epithelial and stromal developmental patterns in a novel substitute of the human skin generated with fibrin-agarose biomaterials. Cells Tissues Organs. 2012;196(1):1–12.
- Alaminos M, Sánchez-Quevedo MDC, Muñoz-Ávila JI, Serrano D, Medialdea S, Carreras I, et al. Construction of a complete rabbit cornea substitute using a fibrin-agarose scaffold. Investig Ophthalmol Vis Sci. 2006;47(8):3311–7.
- Sanchez-Quevedo MC, Alaminos M, Capitan .L.M., Moreu G, Garzon I, Crespo PV, et al. Histological and histochemical evaluation of human oral mucosa constructs developed by tissue engineering. Histol Histopathol. 2007;(22):631–40.
- Carriel V, Scionti G, Campos F, Roda O, Castro B, Cornelissen M, et al. In vitro characterization of a nanostructured fibrin agarose bio-artificial nerve substitute. J Tissue Eng Regen Med. 2017 May;11(5):1412–26.
- Nims RJ, Cigan AD, Albro MB, Hung CT, Ateshian GA. Synthesis rates and binding kinetics of matrix products in engineered cartilage constructs using chondrocyte-seeded agarose gels. J Biomech. 2014;47(9):2165–72.
- Awad HA, Wickham MQ, Leddy HA, Gimble JM, Guilak F. Chondrogenic differentiation of adipose-derived adult stem cells in agarose, alginate, and gelatin scaffolds. Biomaterials. 2004;25(16):3211–22.
- Lai ZW, Schilling O. Protein Terminal Profiling. 2017;1574:105–14.
- IHC World. Paraffin Sectioning Methods and Techniques [Internet]. 2013 [cited 2017 May 24]. Available from: http://www.ihcworld.com/_protocols/histology/paraffin_section.htm
- Rodriguez-Arco L, Rodriguez IA, Carriel V, Bonhome-Espinosa AB, Campos F, Kuzhir P, et al. Biocompatible magnetic core–shell nanocomposites for engineered magnetic tissues. Nanoscale. 2016;8(15):8138–50.
- Carriel V, Aneiros-Fernández J, Ruyffelaert M, Arias-Santiago S, Riady V, Izquierdo-Martínez F, et al. Histological and immunohistochemical study of an unusual type of gallbladder duplication. Histol Histopathol. 2014;29(7):957–64.
- Martín-Piedra MA, Garzón I, Oliveira AC, Alfonso-Rodriguez CA, Carriel Araya VS, Scionti G, et al. Cell viability and proliferation capability of long-term human dental pulp stem cell cultures. Cytotherapy. 2014;16(2):266–77.
- Boraas LC, Ahsan T. Lack of vimentin impairs endothelial differentiation of embryonic stem cells. Sci Rep. 2016;6(August):30814.
- Drury JL, Mooney DJ. Hydrogels for tissue engineering: Scaffold design variables and applications. Vol. 24, Biomaterials. 2003. p. 4337–51.
- Chi WJ, Chang YK, Hong SK. Agar degradation by microorganisms and agar-degrading enzymes. Appl Microbiol Biotechnol. 2012;94(4):917–30.
INFORMACIÓN DEL ARTÍCULO
Agradecimientos: Gracias a todos los integrantes del departamento de Histología de la Facultad de Medicina de la Universidad de Granada por permitir la realización de este estudio y por el apoyo recibido.
Autor para la correspondencia: Pedro Quintero Campos. e-mail: pedro.quintero.campos@gmail.com. Teléfono: 664619527. Dirección: Departamento de Histología – Facultad de Medicina – Universidad de Granada