Revisión
Lesiones del ligamento cruzado anterior. Nuevas opciones de tratamiento mediante ingeniería de tejidos
Anterior cruciate ligament injury. New treatment options by tissue engineering
Actual. Med. 2014; 99: (793): 157-161 DOI: 10.15568/am.2014.793.re02
Enviado: 12-09-2014
Revisado: 11-12-2014
Aceptado: 29-12-2014
RESUMEN
Las lesiones del ligamento cruzado anterior (LCA) constituyen una causa frecuente de lesiones en población joven. Al tratarse de una estructura intraarticular, el ligamento cruzado lesionado no cicatriza de forma similar al de otros ligamentos extraarticulares, de forma que entre los cabos de ruptura no se interpone el coágulo de fibrina que aparece en las fases iniciales de la cicatrización. La ruptura del LCA conlleva la aparición de inestabilidad de rodilla, daño meniscal y aparición de artrosis precoz. El tratamiento quirúrgico mediante reconstrucción anatómica con injertos es una técnica eficaz aunque no ha demostrado que prevenga la aparición de artrosis precoz. La ingeniería tisular contribuye al desarrollo de nuevas técnicas de tratamiento basadas en terapia celular, terapia génica, uso de factores de crecimiento y de matriz extracelular para tratar de conseguir una cicatrización del LCA sin necesidad de recurrir al uso de injertos. El uso de una matriz de colágeno impregnada con PRP asociando sutura directa del LCA ha demostrado un buen resultado funcional con una menor tasa de aparición de artrosis al año de seguimiento.
Esta revisión se ha realizado a partir de una búsqueda bibliográfica en pubdmed con las palabras clave tomando los artículos más recientes. El objetivo es poner de manifiesto las nuevas opciones de tratamiento en las lesiones del ligamento cruzado anterior mediante ingeniería de tejidos.
Palabras clave: ligamento cruzado anterior, lesión, reconstrucción, reparación, ingeniería tisular
ABSTRACT
Injuries to the anterior cruciate ligament (ACL) is a common cause of injury in young population. Being an intraarticular structure, the ACL does not heal in a similar manner to other extra-articular ligaments, so the break between the two ends of the injured ACL is not filed with the fibrin clot that appears in the early stages of healing. The ACL tear involves the occurrence of knee instability, meniscal injury and early onset of osteoarthritis. Surgical treatment by anatomic reconstruction with grafts is an effective technique but has not proven to prevent the onset of early osteoarthritis. Tissue engineering contributes to the development of new treatment techniques based on cell therapy, gene therapy, use of growth factors and scaffolds to try to get an ACL healed without the disadvantages of the use of grafts. The use of a collagen matrix impregnated with PRP associating direct suture of the ACL has demonstrated a good functional outcome with a lower rate of presence of osteoarthritis at one year of follow-up.
This review is perfomed by a literature research with the keywords in pubmed taking the most recent articules. The aim is to highlight the new treatment options for lesions of the anterior cruciate ligament using tissue engineering.
Keywords: anterior cruciate ligament, injury, reconstruction, repair, tissue engineering
Leer Artículo Completo
INTRODUCCIÓN
Las lesiones del ligamento cruzado anterior (LCA) constituyen una de las lesiones ligamentosas más frecuentes en el organismo. Suelen producirse en población joven, deportista (fundamentalmente esquiadores y futbolistas) y son más frecuentes en el sexo femenino. (1)
Debido a la incidencia de estas lesiones en jóvenes, el impacto económico y social que acarrean es considerable en términos de costes indirectos derivados del riesgo de presentar complicaciones como inestabilidad, osteoartritis postraumática de rodilla, y aparición de daño meniscal, así como por el elevado coste de su tratamiento (conservador o quirúrgico) (2).
El LCA es una estructura intraarticular compuesta de fibras de colágeno tipo I que se origina en la superficie posterolateral de la escotadura intercondílea del fémur, y discurre en sentido anterodistal para insertarse en una región anterior a la eminencia intercondílea. Se compone de dos fascículos entrecruzados que soportan diferente tensión en función del grado de flexoextensión de la rodilla. La función principal del ligamento consiste en garantizar la estabilidad anterorotatoria de la tibia sobre el fémur. Además, contribuye como propioceptor de la articulación. Estáirrigado por ramas arteriales en íntimo contacto con el ligamento (3).
La lesión del LCA generalmente ocurre cuando se provoca un valgo forzado de la rodilla con rotación interna de la tibia y traslación anterior de la misma. Es frecuente la percepción de un chasquido seguido de derrame articular de rápida instauración (hemartros) y dolor (4).
Se recomienda la realización de radiografías simples para descartar la presencia de lesiones óseas asociadas. La resonancia magnética se emplea para confirmar el diagnóstico de sospecha y establecer una adecuada planificación quirúrgica (5).
Histológicamente, tras la ruptura, el LCA atraviesa cuatro fases histológicas: fase inflamatoria, fase de regeneración epiligamentosa, fase proliferativa y fase de remodelado (6). La respuesta a la lesión es similar a la que ocurre en otros tejidos conectivos con algunas peculiaridades como la ausencia de tejido entre los cabos de ruptura, la formación de una capa de células sinoviales en la superficie de los extremos del ligamento lesionado y la presencia de la fase de regeneración epiligamentosa (7). Estas diferencias se atribuyen al hecho de que el LCA se encuentra inmerso en un microambiente de líquido sinovial que impide la formación de un coágulo que sirva de puente entre los cabos de la ruptura, altera la respuesta inflamatoria y el metabolismo celular (8). Por otro lado, la ruptura del LCA va asociado a la lesión de las ramas vasculares que lo nutren por lo que presenta un insuficiente aporte vascular una vez lesionado. No obstante los estudios histológicos demuestran la existencia de vascularización intraligamentaria en las fases precoces tras la lesión del LCA (9). Los ligamentos extraarticulares de la rodilla son estructuras bien vascularizadas que presentan una fase inflamatoria con formación de un coágulo que permite la cicatrización del mismo (10). A pesar de las diferencias observadas en las fases de cicatrización, los fibroblastos que componen el LCA tienen similar capacidad para la cicatrización que los existentes en el ligamento colateral medial (LCM) de la rodilla (11).
Para abordar el objetivo de esta revisión se ha realizado una búsqueda bibliográfica en pubmed con los términos “anterior cruciate ligament”, “injury”, “reconstruction” , “repair” y “tissue engineering” revisando aquellos artículos más recientes así como los más citados por su relevancia. Se ha prestado especial interés en aquellos artículos que hacían referencia a técnicas de ingeniería tisular como tratamiento de este tipo de lesiones.
TRATAMIENTO ACTUAL DE LAS LESIONES DEL LCA
Las opciones terapéuticas de las que disponemos actualmente en la clínica, son:
TRATAMIENTO CONSERVADOR
El tratamiento conservador incluye la realización de ejercicios de fortalecimiento muscular del cuádriceps y los isquiotibiales. Se reserva para casos de baja demanda funcional, bien por comorbilidad o bien por presentar ocupaciones sedentarias y no realizar práctica deportiva (5). Además, no todas las lesiones del LCA conllevan inestabilidad de rodilla. Un reciente de coste-efectividad en EEUU revela que el tratamiento conservador basado en rehabilitación conlleva mayor gasto económico que la reconstrucción quirúrgica (12). No obstante, en otra revisión sistemática reciente se indica que actualmente no hay argumentos basados en la evidencia que recomienden una reconstrucción sistemática del LCA para los pacientes que se lo lesione (13).
TRATAMIENTO QUIRÚRGICO
La reparación del LCA mediante sutura directa fue descrita por primera vez por Mayo Robson en 1900 (14). A mediados del siglo XX se empleó como técnica quirúrgica de elección. No obstante este procedimiento se abandonó debido a que la tasa de fracaso alcanzaba el 90% a los 5 años de seguimiento (15). Diversos estudios han comparado la eficacia del tratamiento con sutura directa del LCA respecto al tratamiento conservador, sin encontrar diferencias significativas entre ambas opciones (16).
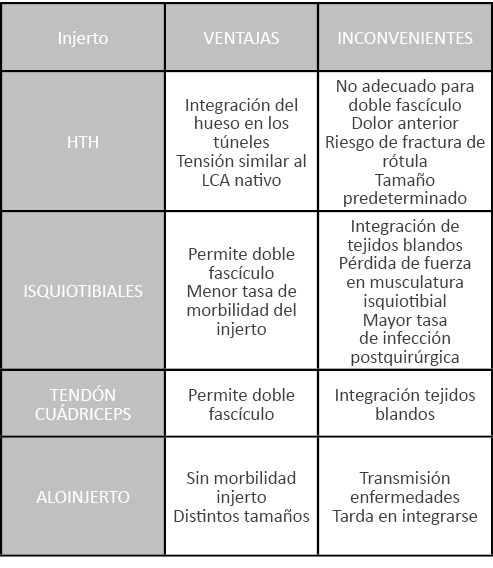
Actualmente el tratamiento de elección de las lesiones del LCA se basa en la reconstrucción quirúrgica mediante el uso de plastias o injertos (17). Se han descritos varias ténicas para crear una estructura que trata de reproducir el LCA mediante injertos. El injerto ideal es aquel que imita la anatomía y las propiedades del LCA. Debe ser capaz de resistir una tensión adecuada, seguir el trayecto anatómico del LCA nativo, garantizar una fijación inicial segura y ser capaz de madurar e integrarse adecuadamente (18). La selección del injerto debe realizarse teniendo en cuenta diversas características (Tabla 1).
Tabla 1. Características de las distintas plastias para la reconstrucción del LCA.
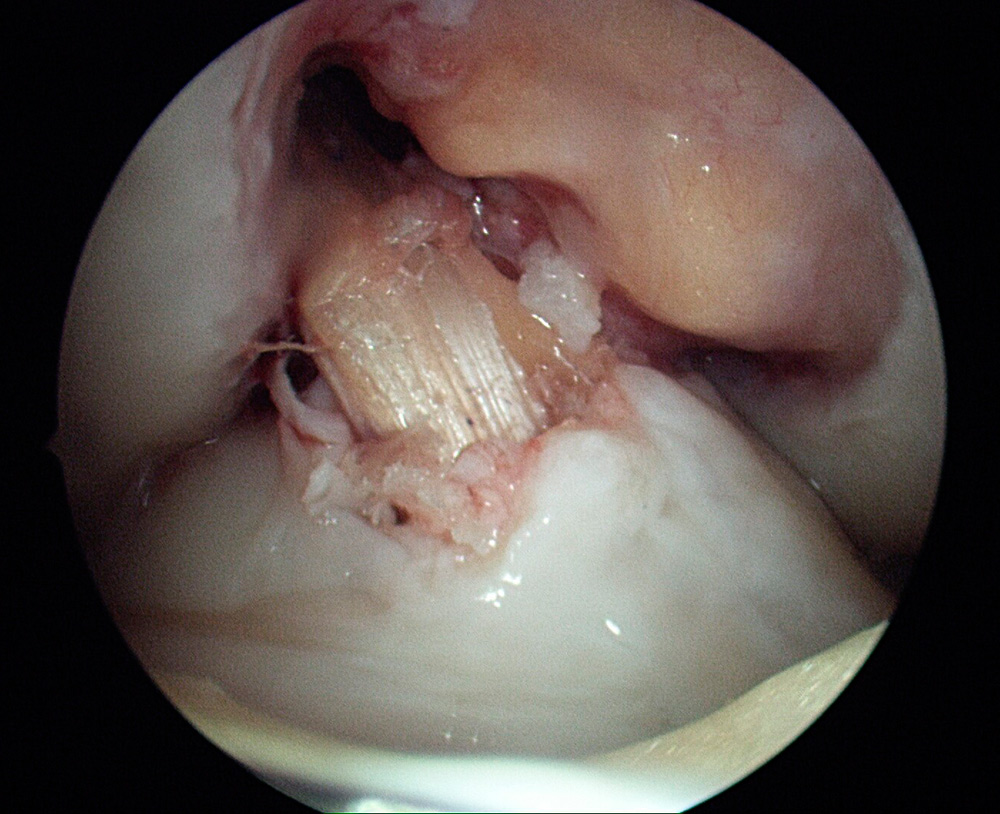
Plastia autóloga hueso – tendón –hueso (HTH): se compone de tendón rotuliano con fragmentos óseos procedentes de la rótula y la tibia. Este tipo de injertos permite una fijación adecuada (integración hueso-hueso) con una tasa baja de fracasos, a pesar de contar con un alto índice de dolor anterior de rodilla con una ligera pérdida de la capacidad de extensión y presentan riesgo de sufrir fracturas de rótula. El tamaño del mismo estápredeterminado. No permite reconstrucción mediante la técnica del doble fascículo (19). (Figura 1)
Figura 1. Visión intraoperatoria de reparación de LCA mediante plastia HTH.
Plastia autóloga tetrafascicular (injerto de isquiotibiales): En contraposición a los injertos HTH presentan una tasa inferior de dolor anterior de rodilla, pero la tasa de fracaso es ligeramente superior. Puede modificarse el tamaño del mismo. La integración se basa en una interacción hueso – tejido blando. Un estudio sugiere que a pesar de que es una técnica segura y eficaz, la tasa de infección postquirúrgica es superior cuando se emplea este tipo de autoinjerto (20). (Figura 2)
Figura 2. Preparación de injerto de tetrafascicular.
Injerto de tendón cuadricipital: permite realizarse bien incluyendo un fragmento óseo rotuliano o bien injerto libre de hueso. Supone una alternativa al uso de plastia de isquiotibiales (21).
Injerto alogénico: La ventaja principal del injerto alogénico es que evita la morbilidad del lugar de extracción del injerto autólogo. Entre los principales inconvenientes cabe destacar el elevado coste, los problemas derivados de la posibilidad de transmisión de enfermedades y fallos en la integración del mismo (22).
Para integrar la plastia es preciso realizar túneles en fémur y tibia y asípermitir el anclaje de la plastia en el hueso. Numerosos estudios han procurado establecer qué técnica para la realización de túneles es más eficaz (túnel transtibial o túnel anteromedial) para garantizar una reconstrucción anatómica. Una revisión sistemática que compara ambas técnicas concluye que la técnica anteromedial pretende garantizar una mejoría en la biomecánica de la rodilla intervenida pero que la técnica transtibial es capaz de producir resultados similares si se realiza correctamente y con algunas modificaciones (23). Otros estudios tratan de establecer correlación mediante el uso de RM para valorar la maduración e integración de la plastia en el organismo y asívalorar el éxito o el fracaso de la plastia (24).
Con el objetivo de conseguir una plastia anatómicamente similar al LCA nativo se ha desarrollado la técnica del doble fascículo. Esta técnica representa una mejora en la estabilidad de la rodilla al trata de imitar la morfología bifascicular del LCA. No obstante no hay evidencias suficientes para recomendar esta técnica respecto a la reconstrucción simple del LCA. Es posible lograr una plastia anatómica utilizando ambas (25).
NUEVAS OPCIONES DE TRATAMIENTO MEDIANTE INGENIERÍA DE TEJIDOS
El empleo de injertos en la reconstrucción del LCA constituye actualmente el gold standard en el tratamiento de las lesiones completas de esta estructura, no obstante, presentan problemas como los descritos en relación a la morbilidad del injerto. Otras limitaciones relevantes del tratamiento quirúrgico son la aparición de artrosis postraumática, pérdida de propiocepción y déficit neuromuscular en la articulación (26).
En una reciente revisión sistemática de la literatura sobre los resultados en la cirugía de reconstrucción del LCA, se ha comprobado que los pacientes que se someten a reconstrucción presentan menos lesiones meniscales, menos cirugías de revisión y una mejoría funcional basada en la escala Tegner (17). Sin embargo, no se observaron resultados significativos en cuanto al desarrollo de artrosis radiológica. Por tanto, algunos estudios advierten de la necesidad de informar a los pacientes que se sometan a tratamiento quirúrgico de LCA que a pesar de la cirugía no va a conseguirse evitar el desarrollo de artrosis (26).
El auge de la ingeniería tisular ha propiciado que se hayan desarrollado alternativas a la reconstrucción mediante injerto del LCA. De conseguir una técnica eficaz mediante ingeniería tisular se lograría una mejora en la biomecánica de la rodilla al preservar el ligamento nativo y se vitarían las complicaciones que presenta la reconstrucción mediante injertos autólogos o heterólogos.
Terapia celular:
Las células madre mesenquimales son capaces de diferenciarse en fibroblastos que permiten la regeneración de los ligamentos y otros tejidos (27). La aplicación de estas células mediante inyecciones intraarticulares en roturas parciales del LCA han demostrado buenos resultados en estudios en ratas (28). Esta técnica precisa de más estudios que avalen el uso de esta terapia para conseguir la diferenciación específica de las células madre mesenquimales en células especializadas en la reparación tisular, asícomo mejorar el desarrollo y mantenimiento de las células en el lugar de la lesión.
Terapia génica:
La transferencia de genes permite, a través del uso de vectores, modular la expresión de factores de crecimiento en las células encargadas de la regeneración tisular modificando la síntesis de proteínas (29). Actualmente hay estudios basados en el uso de vectores virales en conejos con el LCA roto que buscan incrementar la expresión de colágeno y otros factores de crecimiento en las células del LCA, con resultados que muestran incremento en la concentración de estas moléculas durante 6 semanas (30). Otro reciente estudio muestra que las células del LCA tratadas con vectores adenovirales consiguen expresar FGF-2 de forma mantenida que permite aumentar el proceso de curación en las lesiones del LCA en humanos (31). El uso de terapia génica se ve limitado por la necesidad de mantener esta expresión a lo largo del tiempo, y el riesgo potencial de desarrollo de tumores inducidos por los vectores (32).
Factores de crecimiento
Los factores de crecimiento (IGF, TGF, PDGF, VEGF, FGF, NGF) han demostrado ser capaces de regular y mejorar la proliferación celular, el crecimiento de matriz extracelular y de diferenciar a las células madre mesenquimales hacia fibroblastos. Diferentes estudios avalan el uso de estos factores como potenciadores en la reparación de ligamentos dañados (33).
El plasma rico en plaquetas (PRP) ha sido empleado recientemente como tratamiento en distintas lesiones musculoesqueléticas. Este método permite obtener de forma sencilla una alta concentración de factores de crecimiento mediante la separación por centrifugación de las plaquetas y la sangre. El uso de PRP se fundamenta en el hecho de que las plaquetas inicialmente alcanzan el lugar de la lesión y liberan numerosas señales que favorecen la restitución del tejido dañado. Son especialmente relevantes en el desarrollo y producción de fibroblastos y colágeno los factores PDGF y TGF (34). El uso de PRP en el tratamiento de las lesiones del LCA ha sido estudiado por diversos autores que han encontrado mejoras en la reparación de lesiones del LCA in vitro y en modelos animales (35). No obstante un reciente artículo indica que el uso aislado de PRP no es suficiente para promover la cicatrización en cruzados rotos tratados mediante sutura directa (36).
Uno de los principales inconvenientes del uso de factores de crecimiento es la corta duración del efecto que presentan, así como el mantenimiento de los factores en el lugar de la lesión y el desarrollo de técnicas que permitan su reproducción.
Scaffolds, matrices o andamios:
El uso de matrices consiste en la aplicación de estructuras sintéticas o biológicas que han sido utilizadas en medicina regenerativa a modo de soportes de matriz extracelular (37). En el caso del LCA se han empleado diversas matrices de colágeno mostrando resultados prometedores en la regeneración del LCA (38). La submucosa de intestino delgado de cerdo contiene un alto contenido en colágeno asícomo diversas citoquinas y factores de crecimiento útiles para la cicatrización de tejidos conectivos (39). Uno de estos estudios, utilizando una cabra como modelo, indica que a través de una matriz extracelular basada en submucosa de intestino delgado de cerdo se acelera la curación en la sutura directa tras una ruptura controlada del LCA, con una hipertrofia limitada del tejido y cierta mejoría en las propiedades biomecánicas (40). No obstante un estudio reciente indica que el uso de matrices basadas en colágeno de forma aislada no mejoran las propiedades funcionales en LCA tratados mediante sutura directa en modelos animales (41).
Murray (42) ha presentado recientemente estudios que avalan el uso de una matriz extracelular basada en colágeno suplementada con PRP y sutura directa que mejora la reparación del LCA en animales comparado con la sutura directa aislada del LCA lesionado. Esta técnica combinada de matriz extracelular y PRP se fundamenta en la hipótesis de que la reparación espontánea del LCA no se produce debido a la ausencia inicial de hematoma entre los dos extremos del LCA roto por el efecto de lavado que genera el líquido sinovial en el que se halla inmerso el ligamento y al consiguiente déficit de factores de crecimiento que se encuentran en el coágulo. Empleando como modelo el cerdo, realizan un estudio comparando la respuesta a los 6 meses y al año en cerdos en los que se opta por tratamiento mediante sutura directa, reconstrucción quirúrgica mediante aloinjerto HTH, reconstrucción quirúrgica mediante aloinjerto HTH más matriz de colágeno con PRP (“bio-enhanced ACL reconstruction”) y reparación quirúrgica mediante sutura del LCA implementada con matriz de colágeno con PRP (“bio-enhanced ACL repair”). Al año de seguimiento las articulaciones tratadas mediante reparación bioestimulada presentaban menos lesiones cartilaginosas que el resto de grupos de la comparación. Al parecer, esta nueva técnica permite desarrollar un nuevo método de tratamiento menos invasivo que la reconstrucción quirúrgica del LCA que conduce al desarrollo de un ligamento adecuado biomecánicamente asícomo reducir el daño en el cartílago que aparece tras la lesión del LCA.
CONCLUSIONES
Las lesiones del ligamento cruzado anterior ocurren fundamentalmente en población activa y generan un elevado gasto económico a través de gastos indirectos así como complicaciones derivadas de la inestabilidad de rodilla, daño meniscal y aparición de artrosis precoz en jóvenes.
La cicatrización del LCA es ineficaz debido al microambiente de líquido sinovial en el que se encuentra inmerso que impide la aposición de los cabos y la formación de hematoma en la fase inicial de la cicatrización.
El gold standard en el tratamiento de las lesiones quirúrgicas del LCA es la reconstrucción mediante injertos. Sin embargo, no hay evidencias suficientes que indiquen la superioridad del uso de una determinada plastia sobre otra.
A pesar de la eficacia de la reconstrucción quirúrgica no se ha demostrado que la reconstrucción evite el desarrollo de artrosis tras la cirugía.
La ingeniería tisular pretende contribuir al tratamiento de las lesiones del LCA mediante técnicas basadas en la terapia celular, la terapia génica, el uso de factores de crecimiento y el empleo de matrices.
La reparación directa del LCA asociada al empleo de una matriz de colágeno impregnada en PRP es capaz de conseguir un ligamento biomecánicamente similar al de una reconstrucción con autoinjerto además de evitar el desarrollo de artrosis al año de seguimiento.
REFERENCIAS
- Siegel L, Vandenakker-Albanese C, Siegel D. Anterior cruciate ligament injuries: anatomy, physiology, biomechanics, and management. Clin J Sport Med : official journal of the Canadian Academy of Sport Medicine 2012;22:349-55.
- Lohmander LS, Ostenberg A, Englund M, Roos H. High prevalence of knee osteoarthritis, pain, and functional limitations in female soccer players twelve years after anterior cruciate ligament injury. Arthritis Rheum 2004;50:3145-52.
- Flandry F, Hommel G. Normal anatomy and biomechanics of the knee. Sports Med Arthros 2011;19:82-92.
- Benjaminse A, Gokeler A, van der Schans CP. Clinical diagnosis of an anterior cruciate ligament rupture: a meta-analysis. J Orthop Sports Phys Ther 2006;36:267-88.
- Spindler KP, Wright RW. Clinical practice. Anterior cruciate ligament tear. N Eng J Med 2008;359:2135-42.
- Woo SL, Vogrin TM, Abramowitch SD.Healing and repair of ligament injuries in the knee. J Am Acad Orthop Surg 2000;8:364-72.
- Murray MM, Martin SD, Martin TL, Spector M. Histological changes in the human anterior cruciate ligament after rupture. J Bone Joint Surg Am 2000;82-A:1387-97.
- Andersen RB, Gormsen J. Fibrin dissolution in synovial fluid. Acta Rheumatol Scand 1970;16:319-33.
- Arnoczky SP, Rubin RM, Marshall JL. Microvasculature of the cruciate ligaments and its response to injury.An experimental study in dogs. J Bone Joint Surg Am 1979;61:1221-9.
- Frank C, Schachar N, Dittrich D. Natural history of healing in the repaired medial collateral ligament. J Orthop Res 1983;1:179-88.
- Amiel D, Nagineni CN, Choi SH, Lee J. Intrinsic properties of ACL and MCL cells and their responses to growth factors. Med Sci Sports Exerc 1995;27:844-51.
- Mather RC, 3rd, Koenig L, Kocher MS, Dall TM, Gallo P, Scott DJ, et al. Societal and economic impact of anterior cruciate ligament tears. J Bone Joint Surg Am 2013;95:1751-9.
- Delince P, Ghafil D. Anterior cruciate ligament tears: conservative or surgical treatment? A critical review of the literature. Knee Surg Sports Traumatol Arthrosc 2012;20:48-61.
- Robson AW. VI. Ruptured Crucial Ligaments and their Repair by Operation. Ann Surg 1903;37:716-8.
- Feagin JA, Jr., Curl WW. Isolated tear of the anterior cruciate ligament: 5-year follow-up study. The Am J Sports Med 1976;4:95-100.
- Sandberg R, Balkfors B, Nilsson B, Westlin N. Operative versus non-operative treatment of recent injuries to the ligaments of the knee. A prospective randomized study. J Bone Joint Surg Am 1987;69:1120-6.
- Murawski CD, van Eck CF, Irrgang JJ, Tashman S, Fu FH. Operative treatment of primary anterior cruciate ligament rupture in adults. J Bone Joint Surg Am 2014;96:685-94.
- Shelton WR, Fagan BC. Autografts commonly used in anterior cruciate ligament reconstruction. J Am Acad Orthop Surg 2011;19:259-64.
- Steiner ME, Hecker AT, Brown CH, Jr., Hayes WC. Anterior cruciate ligament graft fixation.Comparison of hamstring and patellar tendon grafts. Am J Sports Med 1994;22:240-6; discussion 6-7.
- Maletis GB, Inacio MC, Reynolds S, Desmond JL, Maletis MM, Funahashi TT. Incidence of postoperative anterior cruciate ligament reconstruction infections: graft choice makes a difference. Am J Sports Med 2013;41:1780-5.
- Lee S, Seong SC, Jo CH, Han HS, An JH, Lee MC. Anterior cruciate ligament reconstruction with use of autologous quadriceps tendon graft. J Bone Joint Surg Am 2007;89 Suppl 3:116-26.
- Krych AJ, Jackson JD, Hoskin TL, Dahm DL. A meta-analysis of patellar tendon autograft versus patellar tendon allograft in anterior cruciate ligament reconstruction.Arthroscopy 2008;24:292-8.
- Chalmers PN, Mall NA, Cole BJ, Verma NN, Bush-Joseph CA, Bach BR, Jr. Anteromedial versus transtibial tunnel drilling in anterior cruciate ligament reconstructions: a systematic review. Arthroscopy 2013;29:1235-42.
- Rabuck SJ, Baraga MG, Fu FH. Anterior cruciate ligament healing and advances in imaging. Clin Sports Med 2013;32:13-20.
- Tiamklang T, Sumanont S, Foocharoen T, Laopaiboon M. Double-bundle versus single-bundle reconstruction for anterior cruciate ligament rupture in adults. Cochrane Database Syst Rev 2012;11:CD008413.
- Chalmers PN, Mall NA, Moric M, Sherman SL, Paletta GP, Cole BJ, et al. Does ACL reconstruction alter natural history?: A systematic literature review of long-term outcomes. J Bone Joint Surg Am 2014;96:292-300.
- Caplan AI. Mesenchymal stem cells. J Orthop Res 1991;9:641-50.
- Kanaya A, Deie M, Adachi N, Nishimori M, Yanada S, Ochi M. Intra-articular injection of mesenchymal stromal cells in partially torn anterior cruciate ligaments in a rat model. Arthroscopy 2007;23:610-7.
- Huard J, Li Y, Peng H, Fu FH. Gene therapy and tissue engineering for sports medicine. J Gene Med 2003;5:93-108.
- Hildebrand KA, Deie M, Allen CR, Smith DW, Georgescu HI, Evans CH, et al. Early expression of marker genes in the rabbit medial collateral and anterior cruciate ligaments: the use of different viral vectors and the effects of injury. J Orthop Res 1999;17:37-42.
- Madry H, Kohn D, Cucchiarini M. Direct FGF-2 gene transfer via recombinant adeno-associated virus vectors stimulates cell proliferation, collagen production, and the repair of experimental lesions in the human ACL. Am J Sports Med 2013;41:194-202.
- Crystal RG. Transfer of genes to humans: early lessons and obstacles to success. Science 1995;270:404-10.
- Moreau JE, Chen J, Bramono DS, Volloch V, Chernoff H, Vunjak-Novakovic G, et al. Growth factor induced fibroblast differentiation from human bone marrow stromal cells in vitro. J Orthop Res 2005;23:164-74.
- Hsu WK, Mishra A, Rodeo SR, Fu F, Terry MA, Randelli P, et al. Platelet-rich plasma in orthopaedic applications: evidence-based recommendations for treatment. J Am Acad Orthop Surg 2013;21:739-48.
- Muller B, Bowman KF, Jr., Bedi A. ACL graft healing and biologics. Clin Sports Med 2013;32:93-109.
- Murray MM, Palmer M, Abreu E, Spindler KP, Zurakowski D, Fleming BC. Platelet-rich plasma alone is not sufficient to enhance suture repair of the ACL in skeletally immature animals: an in vivo study. J Orthop Res 2009;27:639-45.
- Drury JL, Mooney DJ. Hydrogels for tissue engineering: scaffold design variables and applications. Biomaterials 2003;24:4337-51.
- Altman GH, Horan RL, Weitzel P, Richmond JC. The use of long-term bioresorbable scaffolds for anterior cruciate ligament repair. J Am Acad Orthop Surg 2008;16:177-87.
- Badylak SF, Tullius R, Kokini K, Shelbourne KD, Klootwyk T, Voytik SL, et al. The use of xenogeneic small intestinal submucosa as a biomaterial for Achilles tendon repair in a dog model. J Biomed Mater Res 1995;29:977-85.
- Fisher MB, Liang R, Jung HJ, Kim KE, Zamarra G, Almarza AJ, et al. Potential of healing a transected anterior cruciate ligament with genetically modified extracellular matrix bioscaffolds in a goat model. Knee Surg Sports Traumatol Arthrosc 2012;20:1357-65.
- Fleming BC, Magarian EM, Harrison SL, Paller DJ, Murray MM. Collagen scaffold supplementation does not improve the functional properties of the repaired anterior cruciate ligament. J Orthop Res 2010;28:703-9.
- Murray MM, Fleming BC. Use of a bioactive scaffold to stimulate anterior cruciate ligament healing also minimizes posttraumatic osteoarthritis after surgery. Am J Sports Med 2013;41:1762-70.
INFORMACIÓN DEL ARTÍCULO
Autor para la correspondencia: Víctor Bolívar Arroyo. email: vbolivar88@gmail.com