Original
Etiología microbiana y sensibilidad a los antibióticos de las infecciones urinarias en pacientes de la Unidad de Rehabilitación de un hospital regional
Etiology and susceptbility to antimicrobials of urinary tract infections in patients of Rehabilitation Unit of a regional hospital
Actual. Med. 2013; 98: (790): 131-135
Enviado: 28-08-2013
Revisado: 27-10-2013
Aceptado: 15-11-2013
RESUMEN
Objetivos: Conocer los resultados del estudio microbiológico de las muestras de orina de pacientes de la Unidad de Rehabilitación de un hospital regional, incluyendo los datos locales de sensibilidad antibiótica.
Material y métodos: Se analizó la base de datos del Laboratorio de Microbiología del Hospital Universitario Virgen de las Nieves con los estudios microbiológicos de las muestras de orinas realizados durante el año 2012. Se investigó la etiología y la sensibilidad a los antibióticos de los uropatógenos más frecuentes presentes en 143 muestras de orina obtenidas mediante sondaje o cateterismo. Los resultados del estudio de 9066 muestras de orina de micción media de sujetos estudiados en Atención Primaria fueron utilizados como grupo control.
Resultados: El 50% de los pacientes neurológicos presentaron urocultivos positivos, frente al 23% de los controles. E. coli fue el microorganismo más frecuentemente aislado en el grupo de enfermos neurológicos, al igual que en los controles. En el estudio de resistencias E. coli presentó altas tasas de resistencia a ampicilina, cotrimoxazol, ciprofloxacino y amoxicilina con ácido clavulánico.
Conclusiones: E. coli es el microorganismo más frecuentemente aislado en los dos grupos de pacientes estudiados. Las resistencias a los antibióticos de los microorganismos procedentes de los dos grupos tienen patrones diferentes, siendo globalmente menor a fosfomicina.
Palabras clave: Infección urinaria, bacterias, resistencias, antibióticos, vejiga neurógena, urocultivos.
ABSTRACT
Objectives: Knowing the results of microbiological tests of urine samples of patients from the Rehabilitation Unit of a regional hospital, including local data of antibiotic susceptibility.
Material and methods: We analyzed the database of the Microbiology Laboratory of the Hospital Universitario Virgen de las Nieves with microbiological studies conducted urine samples during 2012. We investigated the etiology and antimicrobial susceptibility of uropathogens frequently present in 143 urine samples. The 9066 survey results voiding urine mean in Primary Care study subjects were used as controls.
Results: The 50% of neurological patients had positive urine cultures, versus 23% of controls. E. coli was the most frequently isolated organism group neurological patients, as in the controls. Resistance studies in E. coli showed high rates of resistance to ampicillin, cotrimoxazole, ciprofloxacin and amoxicillin with clavulanic acid.
Conclusions: E. coli is the most frequently isolated microorganism in both groups of patients studied. The antibiotic resistance of microorganisms from the two groups have different patterns, being globally less to fosfomycin.
Keywords: Urinary tract infection, bacteria, resistance, antibiotics, neurogenic bladder, urocultures.
Leer Artículo Completo
Introducción
En los pacientes con vejiga neurógena, secundaria a una lesión medular, esclerosis múltiple, lesión cerebral o mielomeningocele, el riesgo de padecer infección urinaria (IU) aumenta debido a problemas estructurales y fisiológicos de las vías urinarias. También influye el método de evacuación urinaria, por la utilización frecuente de sonda vesical permanente (SVP) y la instrumentación invasiva (1). Se calcula una incidencia media de 2,5 infecciones/paciente/año y es muy frecuente observar estas infecciones en los pacientes de centros de larga estancia. En su tratamiento se consideran como IU complicada por ocurrir en sujetos con patología urológica subyacente (2). Constituyen un problema importante de salud pública por su frecuencia, morbilidad y ser una causa del aumento de las resistencias a los antibióticos de los microorganismos implicados (3). Estos proceden de su propia biota, modificada por la presión ambiental y el uso masivo de antibióticos (4). El mecanismo más frecuente para la infección es el ascendente, desde la uretra. Los microorganismos acceden durante la inserción del catéter, por vía intraluminal, a través de la luz de la sonda, o extraluminal, a través del espacio entre la sonda y la uretra. En la patogenia es fundamental la capacidad de formación del biofilm, donde el crecimiento bacteriano es más lento y las bacterias se vuelven más resistentes a los antibióticos (5). El microorganismo más frecuente es, al igual que en las IU adquiridas en la comunidad sin factores de riesgo, Escherichia coli. Pero podría aumentar la frecuencia de otros bacilos gramnegativos más resistentes a los antibióticos, y los enterococos (2). La presión antibiótica que sufren estos pacientes al estar expuestos a ciclos largos y repetidos de antibióticos puede hacer que aumente el riesgo de infección por bacterias multirresistentes, por lo que el tratamiento empírico de este tipo de infecciones se complica. En este sentido estos pacientes podrían presentar con mayor frecuencia infecciones por microorganismos multirresistentes, como las cepas de bacilos gramnegativos productoras de betalactamasas de espectro extendido (BLEE). Esto conlleva dificultades asociadas al tratamiento de la IU, principalmente a la hora de prescribir un tratamiento empírico en la comunidad (6). El tratamiento antibiótico dependerá de la gravedad del paciente y del riesgo de microorganismos multirresistentes. Es importante solicitar siempre urocultivo y antibiograma, para adaptar el tratamiento a la evolución clínica, y basar el tratamiento empírico en los datos locales de sensibilidad antibiótica que los microbiólogos deben proporcionar periódicamente (2).
La IU en la comunidad es causa frecuente de consulta, especialmente en mujeres en edades de máxima actividad sexual, durante la menopausia y posmenopausia, y en varones a partir de los 50 años; no obstante, el espectro de patógenos en las infecciones no complicadas es limitado, siendo E. coli el microorganismo más frecuentemente aislado. La presencia en dichos grupos de pacientes de cepas productoras de BLEE es variable, aunque se ha constatado un aumento de la incidencia de dichos aislamientos, fundamentalmente de E.coli, siendo en su mayor parte de origen intrahospitalario, pero también adquiridas en la comunidad y en pacientes no portadores de SVP (7).
En este trabajo se analizan los resultados del estudio microbiológico de las muestras de orinas de pacientes de la Unidad de Rehabilitación de un hospital regional, incluyendo los datos locales de sensibilidad antibiótica.
Material y métodos
Entre enero y diciembre de 2012 se procesaron 9209 muestras de orina, sin seleccionar por la patología del enfermo, mediante un protocolo de trabajo previamente establecido en el laboratorio (8) en el que se incluyó el uso del citómetro Sysmex UF-1000i como método de cribado. La detección microbiológica se realizó en 143 muestras recibidas consecutivamente en el laboratorio, procedentes de la Unidad de Rehabilitación del Hospital Universitario Virgen de las Nieves de pacientes con vejiga neurógena; y 9066 muestras procedieron de los servicios clínicos de Atención Primaria del Área de influencia del Hospital. Este es un centro de referencia en la región de Andalucía, al sur de España, y sirve como Hospital General a una población de unos 440000 individuos.
Las muestras procedentes de la Unidad de Rehabilitación correspondieron a pacientes hospitalizados, sondados o cateterizados (100 varones y 43 mujeres); y las de la comunidad correspondieron a 2200 varones y 6866 mujeres no embarazadas, no sondados ni cateterizados.
Las muestras fueron obtenidas mediante técnica del chorro medio, exceptuando en los pacientes sondados, donde se recurrió al pinzamiento de la sonda, y cateterizados, que se obtuvo en el momento de la cateterización. En todos los casos, se utilizaron contenedores estériles o tubos con ácido bórico como conservante (Vacutainer®, Becton Dickinson, Franklin Lakes, NJ). Éstos fueron refrigerados y procesados en las primeras 24 h de acuerdo con los procedimientos descritos previamente (9).
Las muestras, determinadas como positivas en el cribado mediante Sysmex (por tener >150 partículas bacterianas/µL o > 50 células que asemejan a levaduras/µL, de acuerdo con los puntos de corte establecidos previamente) (8), fueron sembradas en el medio CHROMagar Orientation® (Becton Dickinson) utilizando un asa calibrada de 1μL (COPAN, Brescia, Italia). Se realizó el recuento de microorganismos uropatógenos, clasificándose de la siguiente manera (10): negativo (<10000 CFU/mL); presuntivo (entre 10000 y 100000 UFC/mL de dos uropatógenos o uno solo sin leucocituria); significativo (bacteriuria o candiduria con un recuento ≥100000 UFC/mL de uno o dos uropatógenos; o entre 10000 y 100000 UFC/mL de uno sólo con leucocituria); o flora mixta (≥10.000 UFC/mL de más de dos uropatógenos). Los medios fueron incubados durante 24horas a 37ºC.
Las colonias fueron identificadas y estudiadas su sensibilidad por el método de microdilución en caldo mediante el sistema automatizado Microscan Walkaway® (Siemens Healthcare Diagnostics, Munich, Germany). Los antibióticos testados para las enterobacterias fueron: Ampicilina, Amoxicilina con ácido clavulánico, Cefuroxima, Cefotaxima, Cefepime, Gentamicina, Tobramicina, Imipenem, Nitrofurantoína, Ciprofloxacina, Cotrimoxazol y Fosfomicina; para Pseudomonas: Piperacilina-tazobactan, Ceftazidima, Cefepime, Gentamicina, Tobramicina, Amikacina, Imipenem, Meropenem, Ciprofloxacina y Fosfomicina; para Acinetobacter baumanii: Piperacilina-tazobactan, Ceftazidima, Cefepime, Gentamicina, Tobramicina, Amikacina, Imipenem, Meropenem, Ciprofloxacina, Ampicilina-sulbactan y Colistina; para Enterococcus: Ampicilina, Levofloxacina, Nitrofurantoína, Fosfomicina, Vancomicina y Teicoplanina; para Streptococcus: Ampicilina, Vancomicina y Teicoplanina; para Staphylococcus: Cloxacilina, Levofloxacina, Gentamicina, Nitrofurantoína, Cotrimoxazol, Fosfomicina, Vancomicina y Teicoplanina.
Las cepas productoras de ß-lactamasa de espectro extendido (BLEE) fueron detectadas por el método de microdilución, estudiando la sinergia entre las cefalosporinas de tercera generación y el ácido clavulánico. En caso necesario se confirmaron mediante el método de E-test. Todas las técnicas de estudio de la sensibilidad se han realizado según las recomendaciones del Clinical and Laboratory Standars Institute (11).
Los valores de incidencia de los microorganismos identificados y los datos de su sensibilidad se describen por el valor numérico obtenido y su frecuencia.
Resultados
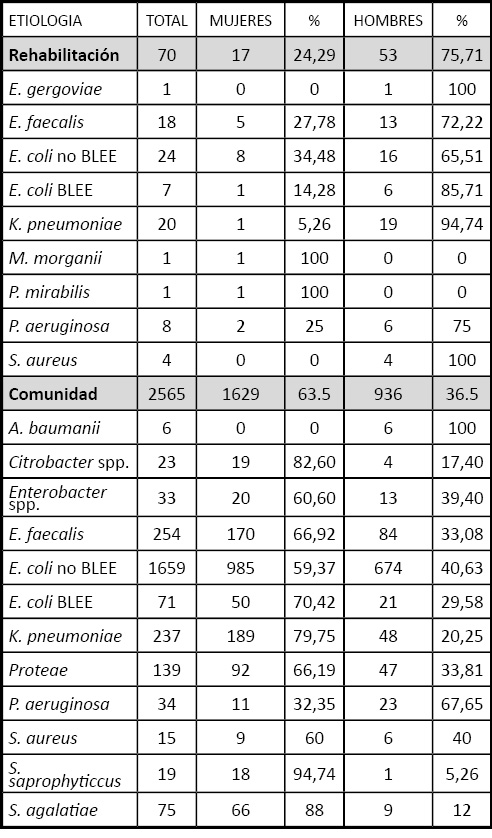
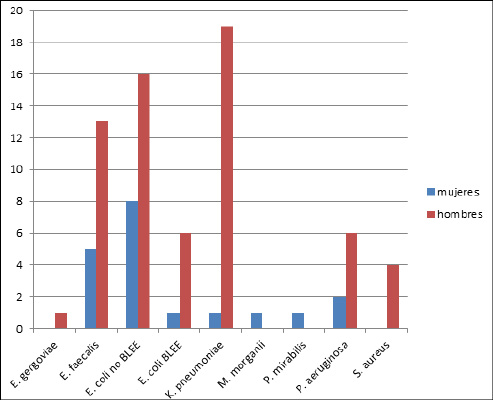
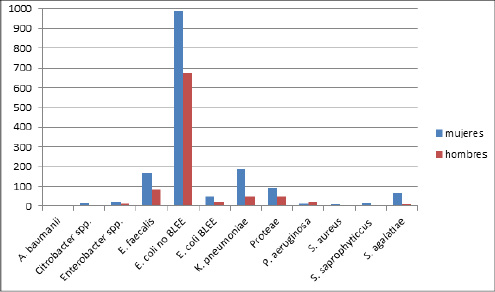
Se obtuvieron 2635 uropatógenos, 1646 (62%) pertenecientes a mujeres y 989 (38%) a hombres (Tabla 1). De los 143 enfermos con lesión neurológica en el 50% de los cultivos estos fueron positivos (el 54% de los varones y el 39% de las mujeres): E. coli fue el más frecuentemente aislado (44%), seguido de Klebsiella pneumoniae (29%), Enterococcus faecalis (26%) y Pseudomonas aeruginosa (11%) (Figura 1). De los enfermos procedentes de Atención Primaria (grupo control) en el 23% de los enfermos el cultivo fue positivo (el 21% de los varones y el 24% de las mujeres): E. coli fue el microorganismo predominante, con una prevalencia del 67%, seguido de E. faecalis (10%) y K. pneumoniae (9%). De forma específica se aislaron Streptococcus agalatiae (3%) y Staphylococcus saprophyticcus (1%). Los bacilos gramnegativos no fermentadores representaron el 1% (Figura 2). Candida no fue aislada en ninguno de los grupos.
Tabla 1. Especies bacterianas aisladas las poblaciones estudiadas y su distribución por sexos.
Figura 1. Microorganismos aislados en los pacientes de la Unidad de Rehabilitación.
Figura 2. Microorganismos aislados en los pacientes de Atención Primaria.
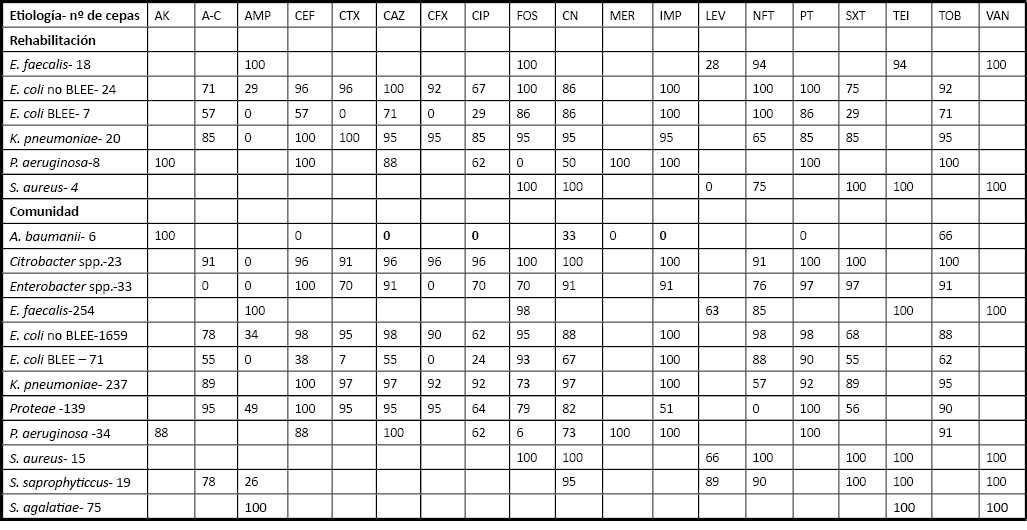
En la Tabla 2 se reflejan los resultados obtenidos en los estudios de sensibilidad a los antibióticos. Se aislaron 78 cepas de E. coli productoras de BLEE (representando el 22.6% de los E. coli en la Unidad de Rehabilitación; y el 4% de los E. coli en Atención Primaria) (Tabla 1). Sólo las cepas productoras de BLEE procedentes de Atención Primaria presentaron resistencia a la cefoxitina en el 20% de los casos. Dichas cepas fueron más resistentes a la fosfomicina en la Unidad de Rehabilitación (14%), a la nitrofurantoína en Atención Primaria (12%), y en ambas localizaciones a ciprofloxacino. La resistencia de E. coli a la ampicilina fue similar: un 73% y un 66%, para la Unidad de Rehabilitación y Atención Primaria, respectivamente; a amoxicilina/ácido clavulánico de un 43% y un 45%, y un 9,1 y 13,3% para cefoxitina, respectivamente. La resistencia a trimetoprim-sulfametoxazol fue superior en los pacientes con E. coli BLEE procedentes de la Unidad de Rehabilitación (71%). La tasa de resistencia a nitrofurantoína fue más alta en las cepas de K. pneumoniae (para la Unidad de Rehabilitación del 37%; para Atención Prmaria del 44%), al igual que para fosfomicina en Atención Primaria (un 29%). No se aislaron Klebsiella pneumoniae productoras de BLEE. Los cuatros aislados de S. aureus de la Unidad de Rehabilitación fueron meticilín resistente, y sólo cinco S. aureus (34%) y S. saprophyticcus (26%) procedentes de Atención Primaria lo fueron. La resistencia a ciprofloxacino fue del 38% en P. aeruginosa. P. aeruginosa en Atención Primaria presentó resistencia a piperacilina/tazobactan en tres aislados (9%) y a imipenem en seis (18%).
El 83% de los Acinetobacter baumannii fueron sensibles a la ampicilina-sulbactam, y todos ellos lo fueron a la colistina. De los enterococos aislados todos correspondían a E. faecalis, con una alta resistencia a quinolonas. Todos fueron sensibles a ampicilina, vancomicina y fosfomicina.
Tabla 2. Resultados obtenidos en los estudios de sensibilidad a los antibióticos en forma de porcentaje de cepas sensibles en el grupo de los pacientes de la Unidad de Rehabilitación y Atención Primaria.
Ampicilina (AMP), Amoxicilina con ácido clavulánico (AC), Cefuroxima (CFX), Cefotaxima (CTX), Cefepime (CEF), Gentamicina (CN), Tobramicina (TOB), Imipenem (IMP), Ciprofloxacina (CIP), Cotrimoxazol (SXT), Fosfomicina (FOS), Piperacilina-tazobactan (PT), Ceftazidima (CAZ), Amikacina (AK), Meropenem (MER), Levofloxacina (LEV), Nitrofurantoína (NFT), Teicoplanina (TEI), Vancomicina (VAN).
Discusión
En el tratamiento de las infecciones del tracto urinario se podría reducir la presión selectiva sobre la biota intestinal y epitelial urogenital si se diversifican los antibióticos y se emplean fármacos específicos para el tratamiento de la infección, de aquí la importancia de conocer los agentes productores y predecir su posible sensibilidad a los antibióticos. Todo lo anterior con lleva a evitar la acumulación de resistencias. El uso frecuente de antibióticos como fosfomicina, con alta actividad frente a E. coli y que no se suele emplear para otras infecciones (12), colaboraría en lo descrito anteriormente.
Al igual que en otras series (13) el microorganismo más frecuentemente aislado es E. coli, en la infección de origen nosocomial y comunitario. En nuestra serie los aislados de E. coli entre los enfermos de Atención Primaria alcanza un porcentaje del 67%, cifra algo inferior a la encontrada por Andreu et al. (14) en infección extrahospitalaria y muy inferior a la obtenida por Gobernado et al. (15). Es probable que la menor cifre de aislados en nuestra seria se deba al aumento de los varones estudiados y estudios para el diagnóstico de ITU postratamiento. En las cepas de E. coli extrahospitalarias destacan las resistencias a ampicilina (66%), cotrimoxazol (32%) y ciprofloxacino (38%).
En los enfermos neurológicos la frecuente hospitalización y el método de evacuación urinaria, principalmente el uso de sondaje y cateterismo, hacen que presenten características que recuerdan a los enfermos hospitalizados, aunque no lo sean en el momento de tener la infección urinaria (16). En nuestra serie se obtuvieron como agentes más frecuentes en lesionados medulares crónicos: E. coli (44.3%), Enterococo (25.7%) y Pseudomonas (11.4%). En los enfermos neurológicos destaca un porcentaje de resistencia a ampicilina (71%) superior a los enfermos comunitarios (66%), pudiendo explicarse este hecho por la mayor presión antibiótica por el uso en aquel grupo de betalactámicos de amplio espectro, ya que existe una correlación significativa entre el consumo de estos fármacos y la resistencia a ampicilina. La resistencias a amoxicilina/ácido clavulánico fueron bastante inferiores: del 29% y 22%, respectivamente. Cefalosporinas de tercera generación y amoxicilina/ácido clavulánico se mantienen con bajas tasas de resistencia en las cepas comunitarias, e incluso en los pacientes neurológicos.
Las resistencias de E. coli a cotrimoxazol son elevadas, aunque variables, y lo descartan en los tratamientos empíricos: en nuestra serie son del 25% en los enfermos neurológicos y del 32% en enfermos comunitarios. Estudios multicéntricos realizados en Norteamérica evidencian también la resistencia de cepas ambulatorias en EE. UU. y Canadá (4). La resistencia a las quinolonas en este estudio es de un 38% en las cepas comunitarias, cifra similar a las descritas en series españolas, que oscilan entre un 18 y un 44%, y próxima a las resistencias de nuestras cepas hospitalarias, donde el porcentaje es del 33%. Está demostrado que la resistencia a quinolonas está ligada claramente al factor geográfico por el consumo excesivo de estas. Normalmente, en las enterobacterias, es el resultado de la mutación cromosómica que causa alteraciones en la diana enzimática y la posterior selección de las cepas resistentes inducida por el abuso del fármaco. Por lo tanto, la razón de este aumento progresivo de resistencia hay que buscarlo en el uso masivo de quinolonas, tanto en humanos como en animales, con variaciones basadas en la edad (la resistencia aumenta con la edad del paciente) y en la región geográfica (4).
Destacan en esta serie las bajas tasas de resistencia a fosfomicina. En nuestra serie la resistencia a la fosfomicina es de hasta el 14% en las cepas de E. coli productoras de BLEE los enfermos neurológicos, y hasta un 30% en las cepas de Enterobacter de los enfermos procedentes de Atención Primaria, cifra que aun siendo relativamente baja es superior a lo que reflejan las series multicéntricas. Su alta actividad intrínseca se explica por su especial farmacocinética, por la adquisición por mutación cromosómica de sus mecanismos de resistencia, y por su falta de uso en la alimentación humana y animal. Esto la convierte en el fármaco ideal para el tratamiento de cistitis no complicadas, siendo también una ventaja la comodidad de su posología (en monodosis o pauta de dos días de 3g). En los últimos años se están realizando estudios sobre la actividad frente a las ITU por cepas productoras de BLEE, siempre que sean cistitis no complicada, con resultados favorables (17). Dichas cepas frecuentemente presentan resistencia cruzada con cotrimoxazol y fluoroquinolonas, y puede obligar a un tratamiento parenteral en enfermos de la comunidad. Por lo tanto, llevan asociado un grave problema terapéutico en el tratamiento de las infecciones urinarias. La eficacia de fosfomicina, de confirmarse en un entorno clínico determinado, significaría una respuesta importante en el tratamiento de las infecciones causadas por este tipo de cepas y evitaría la vía endovenosa para el tratamiento (4). En nuestro nuestro caso resulta ser muy activa frente a estas cepas, en ambos tipos de medios.
Todas las cepas de P. aeruginosa y A. baumanii aisladas fueron sensibles a imipenem, y todos los enterococos aislados eran sensibles a vancomicina. En los enfermos neurológicos hay que tener en cuenta la amplia variedad de microorganismos que pueden causar infección urinaria, lo que dificulta el tratamiento empírico de las ITU, por su especial resistencia a los antibióticos. De los 78 aislados de E. coli BLEE, 7 pertenecen a este grupo (9%), así como todas las cepas de S. aureus fueron meticilín resistente. Entre los grampositivos destacan los enterococos con un 26%. Las altas resistencias a cotrimoxazol y quinolonas en el grupo de los enfermos neurológicos no aconsejan su uso como tratamiento empírico, salvo previa realización de pruebas de sensibilidad a los antibióticos.
En resumen, E. coli es el microorganismo más frecuentemente aislado y fosfomicina parece, en nuestro medio, seguir siendo una posibilidad terapéutica empirica, incluyendo las cepas productoras de BLEE, aunque es aconsejable, siempre que sea posible, realizar urocultivo y estudio de resistencias, lo que permitirá establecer un tratamiento seguro. Las cefalosporinas de 3ª Generación también constituyen una buena alternativa terapéutica limitada al ámbito hospitalario, relegando a un segundo plano a la amoxicilina/ácido clavulánico, cotrimoxazol y ciproflaxacino por su significada tasa de resistencias.
REFERENCIAS
1. Werhagen L, Gabrielsson H, Westgren N, Borg K. Medical complication in adults with spina bifida. Clin Neurol Neurosurg. 2013; en prensa.
2. Pérez-Ayala A, Alós JI. Comentario a ”Urinary infection in patients with neurogenic bladder: patterns of resistance to the most frequent uropathogens”. Actas Urol Esp. 2012; 36:482-3.
3. Xu Y, Moser C, Al-Soud WA, Sørensen S, Høiby N, Nielsen PH, Thomsen TR. Culture-dependent and -independent investigations of microbial diversity on urinary catheters. J Clin Microbiol. 2012; 50: 3901-8.
4. Romero-Cullerés G, Planells-Romeo I, Martinez de Salazar-Muñoz P, Conejero-Sugrañes J. Urinary infection in patients with neurogenic bladder: patterns of resistance to the most frequent uropathogens Actas Urol Esp. 2012;36: 474-81.
5. Djordjevic Z, Jankovic S, Gajovic O, Djonovic N, Folic N, Bukumiric Z. Hospital infections in a neurological intensive care unit: incidence, causative agents and risk factors. J Infect Dev Ctries. 2012;6:798-805.
6. Chitnis AS, Edwards JR, Ricks PM, Sievert DM, Fridkin SK, Gould CV. Device-associated infection rates, device utilization, and antimicrobial resistance in long-term acute care hospitals reporting to the National Healthcare Safety Network, 2010. Infect Control Hosp Epidemiol. 2012;33: 993-1000.
7. Horcajada JP, Shaw E, Padilla B, Pintado V, Calbo E, Benito N, Gamallo R, Gozalo M, Rodríguez-Baño J; The ITUBRAS group; Grupo de Estudio de Infección Hospitalaria (GEIH); Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC). Healthcare-associated, community-acquired and hospital-acquired bacteraemic urinary tract infections in hospitalized patients: a prospective multicentre cohort study in the era of antimicrobial resistance. Clin Microbiol Infect. 2012 Oct 31.
8. Gutiérrez-Fernández J, Lara A, Bautista MF, Luna JD, Polo P, Miranda C, Navarro JM. Performance of the Sysmex Uf1000i system in screening for significant bacteriuria before quantitative culture of aerobic/facultative fast‐growth bacteria in a reference hospital. J Appl Microbiol 2012; 113:609-14.
9. Andreu A, Cacho J, Coira A, Lepe JA. Microbiological diagnosis of urinary tract infections. Enferm Infecc Microbiol Clin 2011; 29: 52-57.
10. Pezzlo M, Mary K. Cork, and Deirdre L. Church. Clinical Microbiology Procedures Handbook Third edition ( Lynne S. Garcia) 2010 ASM Press: Volumen 1 Capitulo 3.12 Urine cultures.
11. Wickler M, Bush K, Cockerill F. Performance Standards for Antimicrobial Susceptibility Testing; Twenty-second Informational Supplement. Wayne, Pennsylvania, USA. 2012.
12. De Cueto M, Hernandez RJ, López Cerezo L, Morrillo C, Pascual A. Actividad de fosfomicina sobre las cepas de E .coli y Klebsiella pneumoniae productoras de betalactamasas de espectro extendido. Enferm Infecc Microb Clin. 2006; 24:613-6.
13. Oteo J, Lazaro E, De Abajo FJ, Baquero F, Campos J. Spanish Member of EARS. Antimicrobial-resistant invasive Escherichia coli, Spain. Emerg Infect Dis. 2005; 11:546-53.
14. Andreu A, Planells I, Grupo Cooperativo Español para el estudio de la sensibilidad antimicrobiana de los patógenos urinarios. Etiología de la infección urinaria baja adquirida en la comunidad y resistencia de Escherichia coli a los antimicrobianos de primera línea. Med Clin (Barc). 2008; 130:481-6.
15. Gobernado M, Valdes L, Alós JL, Garcia Rey C, Dal-Ré R, Garcia-de-Lomas J. The Spain Surveillance Group for Urinary Pathogens. Antimicrobial susceptibily of clinical Escherichia coli isolates from uncomplicated cystitis in women over a 1-year period in Spain. Rev Esp Quimioterap. 2007; 20:68-76.
16. Romero-Cullerés G, Conejero Sugrañes J, Planells Romeo I, Gimenez Pérez M. Características de las infecciones urinarias en diferentes subpoblaciones de pacientes y según sistema de vaciado vesical. Actas Urol Rep 2010; 34:251-7.
17. Rodríguez-Avial C, Rodríguez-Avial I, Hernández E, Picazo JJ. Aumento significativo de la resistencia a fosfomicina en cepas de Escherichia coli productoras de β-lactamasas de espectro extendido (BLEE) aisladas de urocultivos (2005-2009-2011). Rev Esp Quimioter 2013;26:43-46.
INFORMACIÓN DEL ARTÍCULO
Autor para la correspondencia: Dr. José Gutiérrez Fernández. Departamento de Microbiología. Facultad de Medicina. Avda. Madrid, 11 · 18012 Granada. E-mail: josegf@ugr.es