Revisión
Aspectos morfológicos en el desarrollo embrionario: Fragmentación y su relación con la calidad embrionaria. Revisión bibliográfica
Morphological aspects in embryonic development: Fragmentation and its relationship with embryonic quality. Bibliographic review
Actual. Med. 2017; 102: (801): 93-97 DOI: 10.15568/am.2017.801.re02
Enviado: 05-05-2017
Revisado: 30-06-2017
Aceptado: 10-07-2017
RESUMEN
El objetivo de este estudio es hacer una revisión de la fragmentación celular y correlacionarla con la calidad embrionaria. Para ello se realizó una búsqueda sistemática de la literatura sobre «fragmentación embrionaria» y «calidad embrionaria». Para este estudio se incluyeron estudios de parámetros morfológicos por observación convencional asi como los estudios de morfocinética mediante tecnología time-lapse. En primer lugar, se realizó una búsqueda en Cochrane, MEDLINE, MEDES, ENFISPO y EMBASE de todo tipo de artículos (todas las publicaciones hasta diciembre de 2016). Trabajos sobre fragmentación embrionaria, parámetros morfológicos embrionarios y calidad embrionaria, tasa de fragmentación, tasa de implantación y fragmentación embrionaria, morfocinética embrionaria e implantación embrionaria. Se revisaron los resúmenes y se identificaron artículos potencialmente relevantes. De los 50 artículos revisados, 10(20%) fueron ensayos aleatorizados controlados, 21(42%) estudios epidemiológicos observacionales, 8(16%) estudios experimentales, 11(22%) recomendaciones internacionales. Fueron descartados 20(40%) estudios por no ser randomizados y 21(42%) por tratarse de estudios de investigación básica, trabajos de revisión o estudios observacionales. Finalmente se seleccionaron 10(20%) artículos para la revisión por tener relación directa con el objetivo de la revisión. La revisión de los artículos seleccionados relaciona el parámetro de fragmentación embrionaria con otros parámetros morfológicos, no considerándolo como único indicador de una buena calidad embrionaria, valorando el conjunto de los parámetros morfológicos considerado
Palabras clave: fragmentación embrionaria, score fragmentación embrionaria, división celular y fragmentación , desarrollo embrionario y fragmentación, grado de fragmentación, fragmentación embrionaria y time-lapse.
ABSTRACT
The aim of the present study is to review cell fragmentation and to correlate it with embryonic quality. For that, a systematic search of the literature on “embryonic fragmentation” and “embryonic quality” was carried out. For this study, we included morphological parameters researches by conventional observation as well as morphokinetic researches using time-lapse system. First, we searched for all types of articles (all publications until December 2016) in Cochrane, MEDLINE, MEDES, ENFISPO and EMBASE. Moreover, we researched for works on embryonic fragmentation, embryonic morphological parameters and embryonic quality, fragmentation rate, implantation rate and embryonic fragmentation, embryonic morphokinetic and embryonic implantation. Abstracts were reviewed and it was identified potentially relevant articles. Of the 50 articles reviewed, 10 (20%) were randomized controlled trials, 21 (42%) observational epidemiological studies, 8 (16%) experimental studies, 11 (22%) international recommendations; 20 (40%) studies were discarded because they were not randomized and, also, 21 (42%) because they were basic research studies, revision studies or observational studies. Finally, 10 (20%) articles were selected for review because they were directly related to the objective of the review. The review of the selected articles correlates the parameter of embryonic fragmentation with other morphological parameters, not considering it as the only indicator of good embryonic quality, evaluating the set of morphological parameters considered.
Keywords: embryo fragmentation, embryo scoring and fragmentation, cell division and fragmentation, embryo development and cell fragmentation, degree of fragmentation, embryo fragmentation and time-lapse
Leer Artículo Completo
INTRODUCCIÓN
La evaluación morfológica por el embriólogo/a es una metodología no invasiva para el embrión a transferir pero que no está libre de sus desventajas: es altamente subjetivo, requiere gran experiencia y está restringido a momentos puntuales de observación dentro de la rutina del laboratorio, lo cual supone una pérdida de información del desarrollo global del embrión (1)(2). Los principales parámetros a tener en cuenta en la evaluación morfológica del embrión previo al estadio de blastocisto son: número y simetría de las células, grado y tipo de fragmentación, y multinucleación (3)(4). El mecanismo de fragmentación no está todavía clarificado. Parece que hay un efecto debido a una muerte celular programada o apoptosis, que se observa en embriones fragmentados y bloqueados en su desarrollo (5). La fragmentación hace que disminuya la tasa de implantación aumenten las tasas de aborto y de nacimientos de niños con anomalías cromosómicas (6)(7). Lo que es evidente, es que a mayor fragmentación existe un mayor efecto deletéreo y disminución de la viabilidad embrionaria (8).
Un fragmento es una estructura citoplasmática extracelular rodeada por una membrana y sin núcleo en su interior. Algunos autores (9), definieron los fragmentos como células con <45μm de diámetro, en embriones de día 2, y <40μm de diámetro en día 3 de desarrollo (D+3).
Es sabido que la fragmentación puede estar o no presente en todo los estadios del desarrollo embrionario, que es común en todos los embriones humanos y que no siempre se correlaciona con una tasa de implantación baja, por el contrario algunos autores a pesar de no establecer ningún score en su estudio, afirman que la ausencia de fragmentación está relacionado con una alta tasa implantatória, teniendo mayor peso este factor que la multinucleación o baja división embrionaria (Luna, M.D., et al 2008). Otros autores obvian este parámetro morfológico en su clasificación, dando mayor relevancia a la morfología del zigoto en D+1 (7) o bien establecen una clasificación embrionaria en donde prevalece la morfología nuclear por encima de los clásicos métodos basados en el tamaño de las blastómeras y el grado de fragmentación (10), el grupo de Nagy (11) basan la selección embrionaria en los parámetros morfológicos en D+3 conjuntamente a la morfología en 2PN (ver tabla1, resultados).
Las implicaciones de fragmentación embrionaria en el potencial implantatorio varían dependiendo de su distribución y tamaño. La presencia de fragmentos grandes (fragmentación tipo IV) es perjudicial para el desarrollo embrionario, mientras que los fragmentos localizados o pequeños y dispersos no afectan significativamente a la implantación (12). Autores, como Jerome (13), consideran que el grado de fragmentación o porcentaje que pueda presentar el preembrión a transferir no tiene impacto en la tasa de embarazo. Se debe de tener en cuenta que este estudio está realizado para transferencias únicas en mujeres con baja reserva, llegando a la conclusión de que la implantación embrionaria se predice mejor teniendo en cuenta el número y la simetría de las blastómeras frente al grado de fragmentación.
En el desarrollo normal hasta blastocisto la fragmentación tiene un impacto negativo debido a que el tipo de fragmentación determinará la formación de blastocistos normales, concretamente la fragmentación de tipo IV condujo a una reducción significativa en la formación de blastocisto en comparación con otros tipos de fragmentación (tipo I, II y III). (14). Por el contrario el estudio realizado por Wu de 2011(15), establece una correlación negativa entre la tasa de fragmentación y el desarrollo del blastocisto, la edad no tiene un efecto positivo sobre el grado de fragmentación en los preembriones con división correcta. El estudio de Martin de 2006 (16), apoyándose en los estudios de Giorgetti de 1995 (17), el cual consideró que la tasa de embarazo disminuye con el aumento del porcentaje de fragmentos, establecen dos teorías sobre la fragmentación: 1) los fragmentos inducen a la detención del desarrollo celular y a la necrosis de las blastómeras circundantes. 2) los fragmentos intercelulares pueden distorsionar el ritmo de división de las blastómeras, lo que lleva a la anormal compactación, cavitación y formación del blastocisto. El parámetro embriológico que tienen una relación directa con el potencial implantatorio en D+5, es la fragmentación establecida en D+3, aunque es solo una hipótesis por demostrar. Siguiendo la misma línea de estudio el grupo de Khurram (18) consideran que un porcentaje alto de fragmentos (> 20%) en D+3 esta relacionado con bajas tasas de blastulación.
No existe un consenso en cuanto al porcentaje de fragmentos, aunque casi todos los estudios coinciden en un “punto de corte” asociado a la mejor calidad embrionaria y a una tasa mayor de implantación (<10% de fragmentos). En la mayoría de los artículos revisados se establece un score embrionario donde se define unos puntos de corte para la fragmentación embrionaria, expresándola como el porcentaje que ocupa respecto al volumen embrionario total. La mayoría de los autores establecen este punto de corte en < 10% fragmentos (19)(20)(21)(14)(22)(23)(24)(25)(26). Otros autores los establecen en < 25% (13) o en < 20% (18)(23). El estudio de Meseguer (22), establece varias categorías teniendo en cuenta el grado de fragmentación, tamaño de las blastómeras y multinucleación, otros grupos como Paternot de 2013 (27) establecen una clasificación embrionaria a partir de la clasificación computarizada, ya que consideran que existe una alta variabilidad entre embriólogos cuando se realiza la clasificación según características morfológicas visualizadas. Teniendo en cuento estas consideraciones, en cuanto a patrones de fragmentación e implantación embrionaria, la última revisión del Cuaderno Valoración Morfológica ASEBIR (28), establece cuatro grupos de calidad embrionaria, según el porcentaje de fragmentación, volumen y distribución de los fragmentos (≤10%, >10-25%, >25-35%, > 35%), recomendándose que aquellos embriones con más del 50% de fragmentación no deberían de ser criopreservados ni transferidos, debido a que su tasa de implantación es prácticamente nula. Esta última consideración ya la apuntó el estudio de Nagy (23) que afirmaba que para criopreservar el preembrión debe de tener < 20% de fragmentos.
El estudio de la morfocinética embrionario con las nuevas tecnologías de time-lapse, están demostrando que para evaluar la calidad embrionaria deben estudiarse igualmente los mismos parámetros morfológicos que para la observación directa, eso si la morofocinética permite un mayor detalle en la evaluación. Estudios realizados de morfocinética con time-lapse, como el de Kong (29), demuestran que la fragmentación celular y la velocidad de división celular, son parámetros que deben estudiarse conjuntamente como indicadores de la calidad embrionaria, conclusiones que también se obtuvieron otros autores como Ahlstrom (30), en donde los estudios de morfología por observación directa, llegan a la misma conclusión.
La eliminación de fragmentos (embryonic makeup) parece que mejora la división celular y la implantación. El grupo pionero en esta técnica (31) encontró que los embriones con un 35% de fragmentación y que habían sido desfragmentados, implantaban con tasas similares a la de los embriones con sólo un 6% de fragmentación inicial. El trabajo de Keltz (32) también muestra resultados beneficiosos, ya que los embriones fragmentados y posteriormente desfragmentados presentaron tasas de embarazo, implantación y nacimiento similares a la de embriones sin fragmentos (no desfragmentados). Además, la eliminación de fragmentos mostró efectos positivos en el desarrollo in vitro de los embriones hasta el día sexto de su desarrollo, obteniendo blastocistos de mejor calidad (15). No obstante, hay que ser cauteloso en la aplicación de esta técnica, ya que los estudios publicados son escasos y la mayoría de ellos retrospectivos.
MATERIAL Y MÉTODOS
Se realizó una búsqueda sistemática de la literatura sobre «fragmentación embrionaria» y «calidad embrionaria». Para este estudio se incluyeron estudios de parámetros morfológicos por observación convencional asi como los estudios de morfocinética mediante tecnología time-lapse. En primer lugar, se realizó una búsqueda en Cochrane, MEDLINE, MEDES, ENFISPO y EMBASE de todo tipo de artículos (todas las publicaciones hasta diciembre de 2016). Trabajos sobre fragmentación embrionaria, parámetros morfológicos embrionarios y calidad embrionaria, tasa de fragmentación, tasa de implantación y fragmentación embrionaria, morfocinética embrionaria e implantación embrionaria. Se revisaron los resúmenes y se identificaron artículos potencialmente relevantes. Se utilizaron como palabras MeSH de búsqueda: «embryo fragmentation », «embryo scoring and fragmentation», «cell division and fragmentation », «embryo development and cell fragmentation», «degree of fragmentation», «embryo fragmentation and time-lapse». Se encontraron 50 estudios relacionados con los criterios de búsqueda. Se excluyeron los casos clínicos y estudios experimentales. Se revisaron ensayos aleatorizados controlados, estudios comparativos no aleatorizados, estudios epidemiológicos observacionales, recomendaciones o «guidelines» nacionales o internacionales.
Después de identificar los títulos relevantes, se realizó revisión del resumen si el artículo cumplía los criterios de inclusión. Dado que hay una falta significativa de estudios aleatorizados sobre el fragmentación embrionaria y tasa de recién nacido vivo, la valoración de la calidad de la mayoría de los estudios incluidos se basó en la lista de los 7 ítems propuestos por el índice metodológico para estudios no-aleatorizados (MINORS)(33). Todos los artículos se han incluido por su impacto histórico-científico sobre fragmentación embrionaria, calidad embrionaria y tasa de implantación. Las revisiones y artículos editoriales se han incluido por la calidad de las revistas donde fueron publicadas.
RESULTADOS
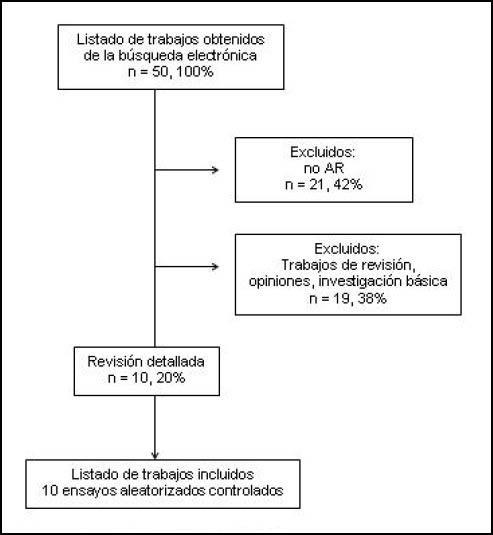
De los 50 artículos revisados, 10(20%) fueron ensayos aleatorizados controlados, 21(42%) estudios epidemiológicos observacionales, 8(16%) estudios experimentales, 11(22%) recomendaciones internacionales. Fueron descartados 20(40%) estudios por no ser randomizados y 21(42%) por tratarse de estudios de investigación básica, trabajos de revisión o estudios observacionales. Finalmente se seleccionaron 10(20%) artículos para la revisión por tener relación directa con el objetivo de la revisión (Figura 1).
Figura 1. Estrategia de búsqueda. Cribado de los trabajos seleccionados para la revisión
La revisión de los artículos seleccionados relaciona el parámetro de fragmentación embrionaria con otros parámetros morfológicos, no considerándolo como único indicador de una buena calidad embrionaria, valorando el conjunto de los parámetros morfológicos considerado (Tabla 1).
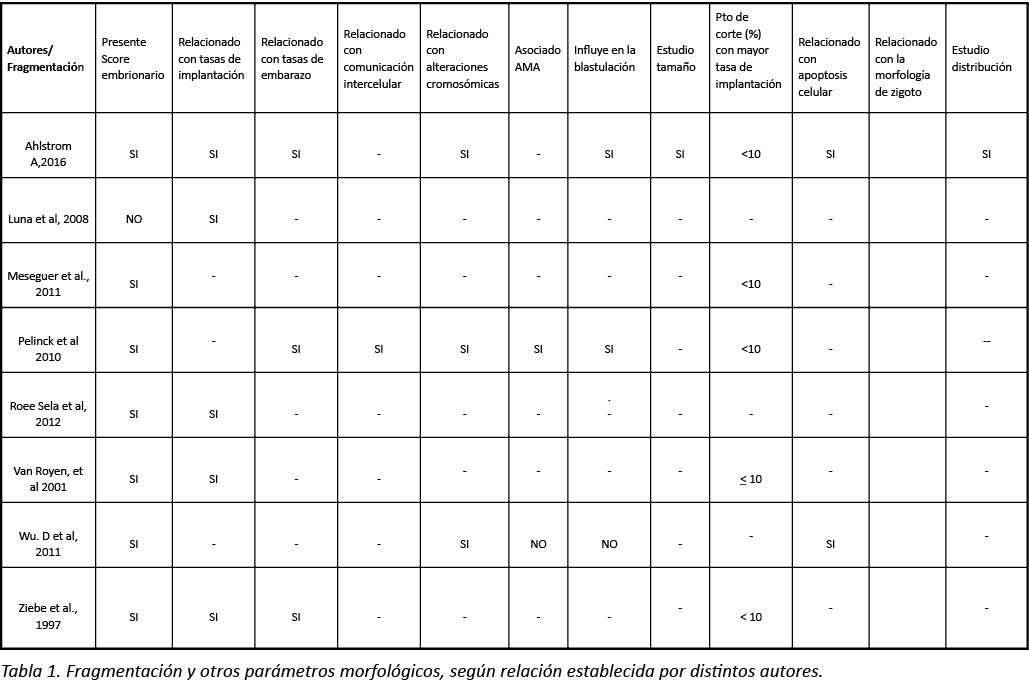
Tabla 1. Fragmentación y otros parámetros morfológicos, según relación establecida por distintos autores
DISCUSIÓN Y CONCLUSIONES
El estudio de la morfocinética embrionaria mediante la tecnología time-lapse, aporta una mayor precisión sobre el comportamiento del embrión durante la división, observándose que el ritmo de división es importante para la implantación (29), cuestiones que no podían ser evaluadas con la evaluación morfológica embrionaria tradicional (observación temporal). A pesar de lo que está aportando el estudio morfocinético mediante la tecnología time-lapse, la calidad embrionaria se define con la evaluación conjunta de los parámetros morfológicos, al igual que ya sucedía con la evaluación morfológica tradicional, si es cierto que el estudio morfocinético, como ya se ha comentada aporta más detalle en la evaluación morfológica. La división temprana conjuntamente con la fragmentación embrionaria, según distintos autores, son indicadores fundamentales para categorizar la calidad del embrión (29). Y se puede seguir afirmando, tras esta revisión, que todos los estudios coinciden en que la fragmentación es un parámetro morfológico importante para establecer la clasificación embrionaria y mayoritariamente se evalúa en D+2 y D+3, casi todos los estudios siguen coincidiendo en un “punto de corte” asociado a la mejor calidad embrionaria y a una tasa mayor de implantación siendo <10% de fragmentos (28).
Todos los estudios revisados coinciden en que este parámetro morfológico es prioritario, debiéndose ser evaluado conjuntamente con otros parámetros morfológicos, a la hora de determinar la calidad embrionaria.
El estudio de la morfocinética mediante la tecnología time-lapse aporta mayor detalle en la evaluación de la fragmentación embrionaria y en general de los parámetros morfológicos.
Cuando la fragmentación es inferior o igual al 10% del volumen celular total (con mejor pronóstico fragmentación localizada a fragmentación dispersa por todo el volumen embrionario) no influye en el potencial implantatorio del preembrión.
Este estudio mantiene los grupos de calidad embrionaria según el porcentaje de fragmentación, volumen y distribución, publicado en 2015 por ASEBIR (28).
REFERENCIAS
- Delgado Mendive M.A. (2016). Relación entre los parámetros morfológicos, de gameto a blastocito, con las anomalías cromosómicas y el éxito reproductivo (Tesis Doctoral). Universidad Complutense de Madrid. Facultad de Veterinaia. Departamento de Medicina y Cirugía Animal. Recuperado de https://www.google.es/?gfe_rd=cr&ei=TNp5WJKOMOKJ8QfN_p64Cg&gws_rd=ssl#q=T37494+tesis
- Delgado A., De Los Santos M., Buendia P., Simon C., Remohi J, & Pellicer A.(2007).Increased incidence of mosaic embryos with the microinjection of spermatozoa with abnormal morphology. Fertil Steril; 88:S229-S230.
- Jurisicova A., Varmuza S., & Casper RF.(1996). Programmed cell death and human embryo fragmentation. Mol Hum Reprod; 2(2):93-8.
- Ebner T., Yaman C., Moser M., Sommergruber M., Pölz W., & Tews G.(2001). Embryo fragmentation in vitro and its impact on treatment and pregnancy outcome. Fertil Steril;76(2):281-5.
- Hardarson, T., Hanson, C., Sjögren, a, & Lundin, K. (2001). Human embryos with unevenly sized blastomeres have lower pregnancy and implantation rates: indications for aneuploidy and multinucleation. Hum Reprod (Oxford, England), 16(2), 313–8. Retrieved from http://www.ncbi.nlm.nih.gov/pubmed/11157826.
- Eftekhari-Yazdi P., Valojerdi MR., Ashtiani SK., Eslaminejad MB., & Karimian L. Effect of fragment removal on blastocyst formation and quality of human embryos. Reprod Biomed Online;13(6):823-32.
- Johansson M., Hardarson T., & Lundin K.(2003).There is a cutoff limit in diameter between a blastomere and a small anucleate fragment. J Assist Reprod Genet;20(8):309-313.
- Luna, M., Copperman, A. B., Duke, M., Ezcurra, D., Sandler, B., & Barritt, J. (2008). Human blastocyst morphological quality is significantly improved in embryos classified as fast on day 3 (>or=10 cells), bringing into question current embryological dogma. Fertil Steril, 89(2), 358–63.
- Chen, C., & Kattera, S. (2006). Comparison of pronuclear zygote morphology and early cleavage status of zygotes as additional criteria in the selection of day 3 embryos: a randomized study. Fertil Steril, 85(2), 347–52.
- Haydar N.Ç., Levent K.,Ulun U., Mustafa B., & Faruk B. (2006). Early cleavage morphology affects the quality and implantation potential of day 3 embryos. Fertility and Sterility, 85(2), 358-365.
- Nagy, Z. P., Dozortsev, D., Diamond, M., Rienzi, L., Ubaldi, F., Abdelmassih, R., & Greco, E. (2003). Pronuclear morphology evaluation with subsequent evaluation of embryo morphology significantly increases implantation rates. Fertil Steril, 80(1), 67–74.
- Alikani, M., M., Cohen, J., Tomkin, G., Garrisi, JG., Mack, C., & Scott, R.(1999). Human embryo fragmentation in vitro and its implications for pregnancy and implantation. Fertil Steril, 71(5), 836–42.
- Jerome H. C., Donna S-C., Wei Y., Danya H., & Carrie W.(2007). Effect of embryo quality on pregnancy outcome following single embryo transfer in women with a diminished egg reserve. Fertility and Sterilit;y 87 (4):749-56.
- Alikani M, Calderón G, Tomkin G, Garrisi J, Kokot M, Cohen J. (2000).Cleavage anomalies in early human embryos and survival after prolonged culture in-vitro. Hum Reprod 2000;15:2634-2643.
- Wu, D. H., Reynolds, K., Maxwell, R., Lindheim, S. R., Aubuchon, M., & Thomas, M. a. (2011). Age does not influence the effect of embryo fragmentation on successful blastocyst development. Fertil Steril, 95(8), 2778–80.
- Martin D. K., Josh C. S.,Katrina B., Daniel S.(2006). Predictors of embryo fragmentation and outcome after fragment removal in in vitro fertilization. Fertil Steril, 86(2), 321–24.
- Giorgetti C., Terriou P., Auquier P., Hans E., Spach J.L., Salzmann J., & Roulier R.(1995). Embryo score to predict implantation after in-vitro fertilization: based on 957 single embryo transfers. Hum Reprod;10(9):2427-31.
- Khurram S. R., Orhan B., Martin L., Bruce R. C., Anna C. N., Kathleen M. D., Kevin J. D.(2007). Late stages of embryo progression are a much better predictor of clinical pregnancy than early cleavage in intracytoplasmic sperm injection and in vitro fertilization cycles with blastocyst-stage transfer. Fertility and Sterility; 87 (5): 1041-52.
- Della Ragione, T., Verheyen, G., Papanikolaou, E. G., Van Landuyt, L., Devroey, P., & Van Steirteghem, A. (2007). Developmental stage on day-5 and fragmentation rate on day-3 can influence the implantation potential of top-quality blastocysts in IVF cycles with single embryo transfer. Reproductive biology and endocrinology: RB&E, 5, 2.
- Hnida, C. (2004). Computer-controlled, multilevel, morphometric analysis of blastomere size as biomarker of fragmentation and multinuclearity in human embryos. Hum Reprod, 19(2), 288–293.
- Holte, J., Berglund, L., Milton, K., Garello, C., Gennarelli, G., Revelli, a, & Bergh, T. (2007). Construction of an evidence-based integrated morphology cleavage embryo score for implantation potential of embryos scored and transferred on day 2 after oocyte retrieval. Hum Reprod (Oxford, England), 22(2), 548–57.
- Meseguer, M., Herrero, J., Tejera, A., Hilligsøe, K. M., Ramsing, N. B., & Remohí, J. (2011). The use of morphokinetics as a predictor of embryo implantation. Hum Reprod (Oxford, England), 26(10), 2658–71.
- Nagy, Z. P., Taylor, T., Elliott, T., Massey, J. B., Kort, H. I., & Shapiro, D. B. (2005). Removal of lysed blastomeres from frozen-thawed embryos improves implantation and pregnancy rates in frozen embryo transfer cycles. Fertil Steril, 84(6), 1606–12.
- Pelinck, M.-J., Hoek, A., Simons, A. H. M., Heineman, M. J., van Echten-Arends, J., & Arts, E. G. J. M. (2010). Embryo quality and impact of specific embryo characteristics on ongoing implantation in unselected embryos derived from modified natural cycle in vitro fertilization. Fertil Steril, 94(2), 527–34.
- Van Royen, E., Mangelschots, K., De Neubourg, D., Laureys, I., Ryckaert, G., & Gerris, J. (2001). Calculating the implantation potential of day 3 embryos in women younger than 38 years of age: a new model. Hum Reprod (Oxford, England), 16(2), 326–32. Retrieved from http://www.ncbi.nlm.nih.gov/pubmed/11157828.
- Ziebe, S., Petersen, K., Lindenberg, S., Andersen, a G., Gabrielsen, a, & Andersen, a N. (1997). Embryo morphology or cleavage stage: how to select the best embryos for transfer after in-vitro fertilization. Hum Reprod (Oxford, England), 12(7), 1545–9. Retrieved from http://www.ncbi.nlm.nih.gov/pubmed/9262293
- Paternot, G., Debrock, S., De Neubourg, D., D`Hooghe, T.M, Spiessens,C. (2013). Semi-automated morphometric analysis of human embryos can reveal correlations between total embryo volume and clinical pregnancy. Hum Reprod (Oxford, England); 28(3): 627–33.
- ASEBIR. (2015). Criterios ASEBIR de Valoración Morfológica de Oocitos, Embriones Tempranos y Blastocistos Humanos 3ª Edición. Madrid. Góbalo.
- Kong X., Yang S., Gong F., Lu C., Zhang S., Lu G., Lin G. (2016). The Relationship between Cell Number, Division Behavior and Developmental Potential of Cleavage Stage Human Embryos: A Time-Lapse Study. PLoS One.14;11(4): e0153697. doi: 10.1371/journal.pone.0153697. eCollection 2016.
- Aisling A., Hannah P., Christina B., Ulrika S., Kersti L.(2016). Conventional morphology performs better than morphokinetics for prediction of live birth after day 2 transfer. Reproductive BioMedicine Online;33:61-70.
- Alikani, M., M., Cohen, J., Tomkin, G., Garrisi, JG., Mack, C., & Scott, R.(1999). Human embryo fragmentation in vitro and its implications for pregnancy and implantation. Fertil Steril, 71(5), 836–42.
- Keltz, M. D., Skorupski, J. C., Bradley, K., & Stein, D. (2006). Predictors of embryo fragmentation and outcome after fragment removal in in vitro fertilization. Fertil Steril, 86(2), 321–4.
- Slim K, Nini E, Forestier D, Kwiatowski F, Panis Y, Chipponi J.(2003). Methodological index for non-randomized studies (MINORS): development and validation of a new instrument. ANZ J Surg;73:712–6.
INFORMACIÓN DEL ARTÍCULO
Autor para la correspondencia: Miguel Angel Vilches Ferrón. Email: mangel.vilches.sspa@juntadeandalucia.es +34 950016165